
����Ŀ���л���F��һ�����ƹؽ���ֹʹҩ���ϳ�F��һ�ִ�ͳ��·����ͼ�� 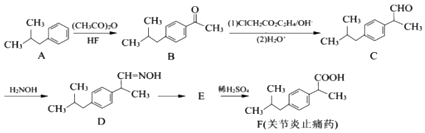
��֪���� ![]() ����
���� ![]() �� ��
�� �� ![]() ��
��
��1��B�к��������ŵ�����Ϊ ��
��2����֪D������Ӧ������E��E�ķ���ʽC13H17N��д��E�Ľṹ��ʽ ��
��3��A��B�ķ�Ӧ����Ϊ��A��B�ķ�Ӧ����ʽΪ ��
��4��д��ͬʱ��������������F��һ��ͬ���칹��Ľṹ��ʽ����дһ�֣���
���ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ���۷�����ֻ��4�ֲ�ͬ��ѧ�������⣮
��5���ϳ�F�� ![]() ����һ�ָ���������2������1��������
����һ�ָ���������2������1�������� ![]() ��������
��������
������[��CH3CO��2O]Ϊԭ�����ϳɣ�д���й�F�ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�
H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH ��
CH3CH2OH ��
���𰸡�
��1���ʻ�
��2��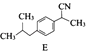
��3��ȡ����Ӧ��![]()
��4��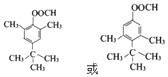
��5��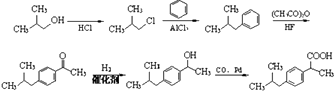
���������⣺A����ȡ����Ӧ����B��B�����ӳɷ�Ӧ����C��C����ȡ����Ӧ����D��D������Ӧ������E��E�ķ���ʽC13H17N������D��F�ṹ��ʽ֪��E�ṹ��ʽΪ 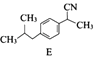 ����1��B�к����������������ʻ������Դ��ǣ��ʻ�����2������E����ʽ��D��F�ṹ��ʽȷ��E�ṹ��ʽΪ
����1��B�к����������������ʻ������Դ��ǣ��ʻ�����2������E����ʽ��D��F�ṹ��ʽȷ��E�ṹ��ʽΪ  �����Դ��ǣ�
�����Դ��ǣ� 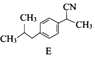 ����3��A����ȡ����Ӧ����B���÷�Ӧ����ʽΪ
����3��A����ȡ����Ӧ����B���÷�Ӧ����ʽΪ ![]() �����Դ��ǣ�ȡ����Ӧ��
�����Դ��ǣ�ȡ����Ӧ�� ![]() ����4��F��ͬ���칹������������������ܷ���������Ӧ��˵������ȩ�������ܷ���ˮ�ⷴӦ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��˵�������������Ȼ����ɷ��ǻ����۷�����ֻ��4�ֲ�ͬ��ѧ�������⣬���������Ľṹ��ʽΪ
����4��F��ͬ���칹������������������ܷ���������Ӧ��˵������ȩ�������ܷ���ˮ�ⷴӦ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��˵�������������Ȼ����ɷ��ǻ����۷�����ֻ��4�ֲ�ͬ��ѧ�������⣬���������Ľṹ��ʽΪ  ��
��
���Դ��ǣ�  ����5������F��ԭ�Ͽ�֪��F�б����ұ����ӵĻ���Ӧ��������������������A��B���پ�����Ϣ�ڵõ��������������2������1������[��CH3��2CHCH2OH��]�����ȱ��±������������Ϣ�ٺϳɣ���������Ϊ��
����5������F��ԭ�Ͽ�֪��F�б����ұ����ӵĻ���Ӧ��������������������A��B���پ�����Ϣ�ڵõ��������������2������1������[��CH3��2CHCH2OH��]�����ȱ��±������������Ϣ�ٺϳɣ���������Ϊ�� 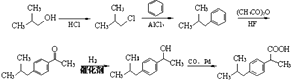 ��
��
���Դ��ǣ� 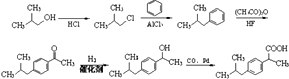 ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��2NO��g��+2CO��g��N2��g��+2CO2��g��
����������ʼ���ʵ����뷴Ӧ�¶����±���ʾ����Ӧ�����мס���������CO2�����ʵ�����ʱ��仯��ϵ����ͼ��ʾ��
���� | �¶�/�� | ��ʼ���ʵ���/mol | |
NO ��g�� | CO ��g�� | ||
�� | T1 | 0.20 | 0.20 |
�� | T1 | 0.30 | 0.30 |
�� | T2 | 0.20 | 0.20 |
����˵����ȷ���ǣ� ��
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.�ﵽƽ��ʱ������CO2����������ȼ��е�С
C.T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2 �� ��Ӧ�ﵽ��ƽ��ǰv��������v���棩
D.T2��ʱ������ʼʱ����г���0.06mol N2��0.12 mol CO2 �� ���ƽ��ʱN2��ת���ʴ���40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵĵ���ƽ�⡢�����ˮ��ƽ�����������ܽ�ƽ������ڻ�ѧƽ�⡣
��.��֪H2A��ˮ�д�������ƽ�⣺H2A=H++HA-��HA-![]() H++A2-
H++A2-
��1��ij�¶��£�����0.1mol��L-1��NaHA��Һ����εμ�0.1 mol��L-1 KOH��Һ����Һ������(���Ի�Ϻ���Һ������仯)����ʱ�û����Һ�е����й�ϵһ����ȷ����__________��
A.c(H+)��c(OH-)=l.0��10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05mol��L-1
��2����֪������H2A�ĸ���(CaA)�ı�����Һ�д�������ƽ�⣺CaA(s)![]() Ca2+(aq)+A2+(aq) ��H>0����Ҫʹ����Һ��Ca2+Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��____________��
Ca2+(aq)+A2+(aq) ��H>0����Ҫʹ����Һ��Ca2+Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��____________��
A.�����¶� B.�����¶�
C.����NH4Cl���� D.����Na2A����
��.����Cr2O72-�ķ�ˮ���Խϴ�ij������ˮ�к�5.0��10-3mol��L-1��Cr2O72-��Ϊ��ʹ��ˮ���ŷŴ�꣬�������´�����
![]()
��1���÷�ˮ�м����̷���H+��������Ӧ�����ӷ���ʽΪ________________________��
��2����������ķ�ˮ�в�����c(Fe3+)=2.0��10-13mol��L-1���������Cr3+��Ũ��Ϊ___________��(��֪��Ksp[Fe(OH)3)]=4.0��10-38�� Ksp[Cr(OH)3]=6.0��10-31)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�������������ij�����غϳɹ����е��м�������˵����ȷ���ǣ� �� 
A.�ҡ������ܷ���������Ӧ
B.��FeCl3��Һ����ס��������л�������
C.����������̼ԭ�ӿ��ܹ�ƽ��
D.�ס��ҡ��������л������������NaOH��Һ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�����������Ȼ�̼�;ƾ��ҵ�����������Ҫ����ˮ�еĵ�������������˵����������
A�������������ɲ��ü��ȵķ����������Һ����������
B�������������Ȼ�̼�;ƾ������Կ�ѡ�������Լ��е�����һ�ֽ�����ȡ
C�����Ȼ�̼��ˮ�أ��ƾ���ˮ�ᣬ���������Ȼ�̼������ȡ���þƾ���
D�����Ȼ�̼������ˮ���ƾ�����ˮ�����������Ȼ�̼��ȡ�������þƾ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ����������ȷ���ǣ� ��
A.��ѧ��������ԭ��֮�䣬Ҳ�ܴ����ڷ���������֮��
B.����ԭ��֮�������ý�����ѧ��
C.���Ӽ�������������֮���������
D.��ѧ��ͨ��ָ����������������ԭ��֮��ǿ�ҵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ���������CO2��CH4�������ƺϳ�������Ҫ�ɷ�ΪCO��H2������֪���������в��ַ�Ӧ���Ȼ�ѧ����ʽΪ��
I��CH4��g���TC��s��+2H2��g����H=+75.0kJmol��1
II��CO2��g��+H2��g���TCO��g��+H2O��g����H=+41.0kJmol��1
III��CO��g��+H2��g���TC��s��+H2O��g����H=��131.0kJmol��1
��1����ӦCO2��g��+CH4��g���T2CO��g��+2H2��g���ġ�H=kJmol��1 ��
��2���̶�n��CO2��=n��CH4�����ı䷴Ӧ�¶ȣ�CO2��CH4��ƽ��ת���ʼ�ͼ�ף� 
��ͬ�¶���CO2��ƽ��ת����������ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����
�ڸ����½��и÷�Ӧʱ������ӦI���ɡ���̼����̼���ʣ�����ɴ����ж��������·�ӦI���Է����е�ԭ���� ��
��3��һ��������Pd��Mg/SiO2������ʹCO2�����黯���Ӷ����Ϊ�����䷴Ӧ������ͼ����ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ
��4��CO�����ڹ�ҵұ����������ͼ���ڲ�ͬ�¶���CO��ԭ���ֽ����������ƽ���������lg[c��CO��/c��CO2��]���¶ȣ�t���Ĺ�ϵ����ͼ������˵����ȷ����
A.��ҵ�Ͽ���ͨ�����߷�Ӧװ�����ӳ���ʯ��
CO�Ӵ���ʱ�䣬����β����CO�ĺ���
B.CO���������ڹ�ҵұ����������Cr��
C.��ҵұ������ͭ��Cu��ʱ�ϵ͵��¶�������
���CO��������
D.CO��ԭPbO2�ķ�Ӧ��H��0
��5�������˺�������Ӧ�õ绯ѧԭ������PtΪ������Pb��CO2�����壩Ϊ������KHCO3��ҺΪ�������Һ����ԭ������������CO2ͬʱ����O2���µ���ԴCO���ܷ�Ӧ�Ļ�ѧ����ʽΪ��2CO2 ![]() 2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G�Ǽ������ķ������ģ��(��ͼ)���ݴ˻ش��������⣺


��1��������������������ȫȼ�գ���������������__________(����ĸ)�������ʵ���������������ȫȼ�գ�����CO2������__________(����ĸ)��
��2����ʹ����KMnO4��Һ��ɫ����_______________(����ĸ)��
��3��G��������ȫ�ӳɺ����ò����һ±������_______�֡�
��4��д��ʵ������ȡD�Ļ�ѧ����ʽ��____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.����һ�����ʵ���Ũ�ȵ���Һ��������ƿ��ˮ��Һ����̶���1��2 cmʱ�����ý�ͷ�ιܶ���
B.��ij��Һ���ȼ���Ba��NO3��2��Һ���ټ���������HNO3��Һ��������ɫ�����������Һ��һ������SO ![]()
C.��Һ����ʱ�����²�Һ���ȷų���Ȼ��ر����������ϲ�Һ����Ͽڵ���
D.����֬������������Һ��ϳ�ַ�Ӧ���ټ����ȵı���ʳ��ˮ�����������������Ҫ�ɷ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com