
【题目】下列关于糖类、蛋白质、油脂的说法中,正确的是
A.它们的组成中都有C、H、O、N等元素
B.在一定条件下,它们都能发生水解反应
C.人体需要的二十多种氨基酸都可以通过人体自身合成
D.油脂都是高级脂肪酸的甘油酯,是一种高热量营养素
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】氯化铜在工农业生产中具有重要的用途。某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2并回收过量的SOCl2。已知:SOCl2的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体。回答下列问题:
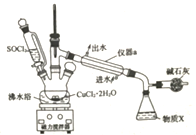
(1)在空气中直接加热CuCl2·2H2O晶体得不到纯净的无水CuCl2的原因是___________________(用化学方程式表示)。
(2)仪器a的名称是____________,锥形瓶中得到的物质x的化学式为______________。
(3)碱石灰中含有CaO和NaOH,NaOH的电子式为__________,碱石灰的作用是______________。
(4)三颈烧瓶中CuCl2·2H2O和SOCl2发生反应的化学方程式是_______________________。
(5)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取 0.2800 g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000 mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O32-=S4O42-+2I-)。
①滴定到终点时的现象是_____________________________________。
②该试样中铜元素的百分含量为__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写不正确的是
A. 钠与水反应:2Na+2H2O=2Na+ + 2OH- +H2↑
B. 电解饱和食盐水获取碱和氯气:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 向碳酸氢铵溶液中加入过量石灰水:Ca2+ +HCO3- +OH-=CaCO3 ↓+H2O
D. 向氢氧化钡溶液中加入稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述中合理的是
A.配制FeCl3溶液,可加入少量稀硫酸,以防止溶液浑浊
B.用25 mL碱式滴定管量取20.00 mL高锰酸钾溶液
C.实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
D.在中和热的测定实验中,改变酸碱的用量后所求中和热的数值也随之改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①小苏打、②硫酸铝、③氯化铁、④磁性氧化铁、⑤氢氧化铁,其中能通过化合反应制得的是( )
A. ①②④⑤B. ①③④⑤C. ②③④⑤D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中 ![]() 和
和 ![]() 代表不同元素的原子.
代表不同元素的原子. 
关于此反应说法错误的是( )
A.一定属于吸热反应
B.一定属于可逆反应
C.一定属于氧化还原反应
D.一定属于分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH <0
2SO3(g) ΔH <0
(1)降低温度,该反应K值______,二氧化硫转化率______。(以上均填“增大”“减小”或“不变”)
(2)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图所示,反应处于平衡状态的时间是______________________。
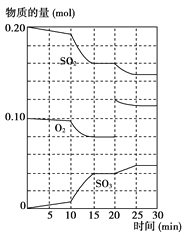
(3)据上图判断,反应进行至20 min时,曲线发生变化的原因是__________________(用文字表达)。
(4)可用上述反应中某种物理量来说明该反应已达到平衡状态的是_______。
A .SO2的生成速率与SO3的生成速率相等
B. 消耗a mol SO2的同时生成a mol SO3
C. 各组分浓度不在发生变化
D.恒容体系中压强不再发生变化
E. 恒容体系中气体密度不再变化
F. ΔH不再发生变化
G.容器里SO2、O2、SO3的浓度比是2:1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com