
【题目】
聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相存性方面有很好的应用前景。 PPG的一种合成路线如下:

已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃:化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④
回答下列问题:
(1)A的结构简式为 。
(2)由B生成C的化学方程式为 。
(3)由E和F生成G的反应类型为 ,G的化学名称为 。
(4)由D和H生成PPG的化学方程式为: 。(3分)
(5)写出D的同分异构体中能同时满足下列条件的有机物结构简式: 。
①能与饱和NaHCO3溶液反应产生气体 ②既能发生银镜反应,又能发生水解反应③核磁共振氢谱显示为3组峰,且峰面积比为6:1:1
(6)D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是_________(填标号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
【答案】(1)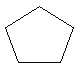
(2)![]()
(3)加成反应;3—羟基丙醛(或β—羟基丙醛)(4)(3分)
![]()
(5) ;
;
(6)c
【解析】试题分析:(1)烃A的相对分子质量为70, 70除以12等于5余数是10,即烃A分子式为C5H10,又因为核磁共振氢谱显示只有一种化学环境的氢,所以结构为 ;(2)A发生光照下取代反应生成B为
;(2)A发生光照下取代反应生成B为![]() ,B发生消去反应生成C为
,B发生消去反应生成C为![]() ,由B生成C的化学方程式为
,由B生成C的化学方程式为![]() ;(3)化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,反应类型为加成反应,G的化学名称为3-羟基丙醛;(4)G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG,化学方程式为:
;(3)化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,反应类型为加成反应,G的化学名称为3-羟基丙醛;(4)G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG,化学方程式为:![]() ;(5既能发生银镜反应,又能发生水解反应,则含有-COOCH结构,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是
;(5既能发生银镜反应,又能发生水解反应,则含有-COOCH结构,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 ;(6)D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同。
;(6)D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据乙烯和乙酸的结构与性质,推测CH2=CH—COOH能发生的反应有( )
①加成反应 ②取代反应 ③氧化反应
A.①②B.②③C.①③D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
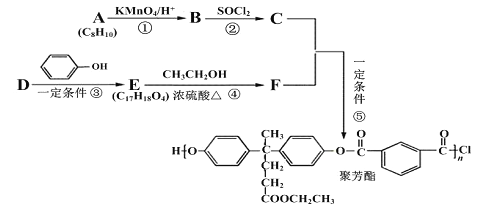
【题目】聚芳酯(PAR)在航空航天等领域具有广泛应用。下图是合成某聚芳酯的路线:
已知: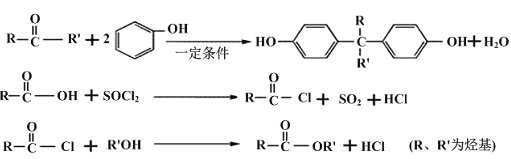
(1)A的名称为______________________,B的结构简式是_________________________。
(2)D的分子式为_______________________,反应④的反应类型是________________。
(3) 写出⑤的化学方程式为______________________________________________。
(4)M是符合下列条件的B的同分异构体
a.能发生银镜反应、水解反应,还能与Na2CO3溶液反应
b.苯环上只有两个取代基且无“—O—O—”结构
c.能与FeCl3发生显色反应
则M共有_______种;其中存在着含4种不同化学环境的氢的物质,写出其与Na2CO3溶液反应但不产生气体的化学方程式(任写一种) ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其化合物在生活和生产中应用广泛。
(1)已知:900 K时,4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。
①该反应是放热还是吸热,判断并说明理由___________________________。
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________

(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:________________________________。
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=________________(用c0、ct表示)mol·L-1。
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO![]() + Cl-
+ Cl-
Ⅱ.ClO![]() +ClO-===ClO
+ClO-===ClO![]() +Cl-
+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体粉末中可能含有SiO2、Fe2O3、CuO、NaHCO3、K2CO3,某同学设计并完成如下实验:(所加试剂均过量)

已知:蘸取少量溶液2在酒精灯上灼烧,透过蓝色钴玻璃观察火焰呈紫色。
请回答:
(1)白色沉淀是__________________(填化学式)。
(2)生成红褐色沉淀的离子方程式为______________________。
(3)根据实验现象, 固体粉末中一定存在的组分是___________________________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是
A. M的分子式为C6H12O6 B. N的结构简式为CH3COOH
C. ④的反应类型属于取代反应 D. 淀粉与纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)、镍(Ni)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用。
(1)Fe2(SO4)3和明矾一样也具有净水作用,其净水的原理是__________________(用离子方程式表示)。
(2)已知某溶液中,Co2+、Ni2+的浓度分别为0.6 mol/L和1.2 mol/L ,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中![]() 的值等于_____。
的值等于_____。
(已知Ksp[Co(OH)2]=6.0×10-15,Ksp[Ni(OH)2]=2.0×10-15)
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。
已知高铁酸盐热稳定性差,工业上用湿法制备K2FeO4的流程如下图所示:

①上述氧化过程中,发生反应的离子方程式是: _________________________,
在实际生产中一般控制反应温度30℃以下,其原因是:
________________________________________________________。
②反应③加入浓KOH溶液可析出高铁酸钾(K2FeO4),这说明________________。
③某温度下,将Cl2通入NaOH溶液中,反应后得到NaCl、NaClO、NaClO3的混合溶液, 经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为______________。
(4)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应式为___________________;其中可循环使用的物质____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是
A.Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.硫化钠的水解反应:S2-+H3O+![]() HS-+H2O
HS-+H2O
D.将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 溴水中当加入硝酸银溶液后,溶液颜色变浅 B. 高压比常压有利于工业合成氨反应
C. 红棕色NO2加压后颜色比原来要深 D. 热的纯碱除油污效果好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com