
【题目】莫沙朵林F是一种镇痛药,可通过木聚糖A按以下路线合成:

(1)有机物B中官能团的名称为____________________。有机物C中的碳碳双键如何检验____________________。
(2)写出同时满足下列条件的E的一种同分异构体的结构简式__________________________。
Ⅰ.存在四种不同化学环境的氢原子;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应。
(3)已知E+X→F为加成反应,写出该反应的化学方程式______________________________。
(4)已知:![]()
![]()
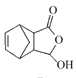
![]() 。化合物
。化合物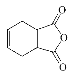 是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以
是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以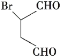 和
和![]() 为原料合成该化合物(用合成路线流程图表示,并注明反应条件)。_____________
为原料合成该化合物(用合成路线流程图表示,并注明反应条件)。_____________
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]() 。
。
【答案】醛基、羟基 取少量C于试管中,先加入银氨溶液,加热,然后酸化后滴入溴水,震荡,溶液褪色,证明含有碳碳双键 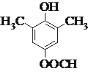 或
或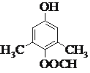
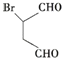
 +O=C=N→
+O=C=N→
【解析】
(1)化合物B中含氧官能团为醛基和羟基;可以用溴水检验碳碳双键,但溴水可以氧化醛基,应先用银氨溶液氧化醛基后再用溴水检验;
(2)E的不饱和度为5,E的一种同分异构体能与FeCl3溶液发生显色反应,说明含有酚羟基;能发生银镜反应和水解反应,含有甲酸形成的酯基(-OOCH),存在四种不同化学环境的氢原子,-OH与-OOCH处于对位,另外还有2个-CH3,分别与-OH相邻,或者分别为-OOCH相邻;
(3)已知E+X→F为加成反应,对比E与F的结构可知X为O=C=N-CH3;
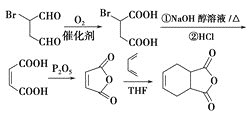
(4) 发生催化氧化生成
发生催化氧化生成![]() ,然后发生消去反应生成
,然后发生消去反应生成![]() ,然后发生取代反应生成
,然后发生取代反应生成![]() ,最后与
,最后与![]() 作用生成
作用生成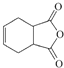 。
。
(1)化合物B中含氧官能团为醛基和羟基;检验C中碳碳双键方法为:取少量C于试管中,先加入银氨溶液,加热,然后酸化后滴入溴水,振荡,溶液褪色,证明含有碳碳双键,故答案为:醛基、羟基;取少量C于试管中,先加入银氨溶液,加热,然后酸化后滴入溴水,振荡,溶液褪色,证明含有碳碳双键;
(2)E的不饱和度为5,E的一种同分异构体能与FeCl3溶液发生显色反应,说明含有酚羟基;能发生银镜反应和水解反应,含有甲酸形成的酯基(OOCH),存在四种不同化学环境的氢原子,OH与OOCH处于对位,另外还有2个CH3,分别与OH相邻,或者分别为OOCH相邻,符合条件的同分异构体结构简式为: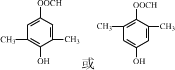 ,故答案为:
,故答案为: ;
;
(3)已知E+X→F为加成反应,对比E与F的结构可知X为O=C=NCH3,该反应的化学方程式为: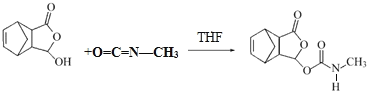 ,故答案为:
,故答案为: ;
;
(4) 发生催化氧化生成
发生催化氧化生成![]() ,然后发生消去反应生成
,然后发生消去反应生成![]() ,然后发生取代反应生成
,然后发生取代反应生成![]() ,最后与
,最后与![]() 作用生成
作用生成 ,合成路线流程图为:
,合成路线流程图为: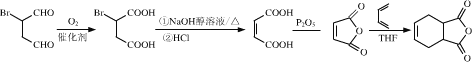 ,故答案为:
,故答案为: 。
。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g) + I2(?)![]() 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?)![]() 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
A.①中的I2为固态,②中的I2为气态
B.②的反应物总能量比①的反应物总能量低
C.①的产物比反应②的产物热稳定性更好
D.1mol 固态碘升华时将吸热17kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,Ca(OH)2在水溶液中达到溶解平衡:![]() 。下列叙述正确的是
。下列叙述正确的是
A.加入少量氢氧化钠固体,Ca(OH)2溶解平衡向左移动,溶液中c(H+)减小
B.加水,Ca(OH)2的溶解平衡向右移动,pH增大
C.加入少量盐酸,Ca(OH)2溶解平衡向右移动Ksp[Ca(OH)2]增大
D.升高温度,Ca(OH)2溶解平衡向右移动,Ksp[Ca(OH)2]增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系,下列有关物质的推断错误的是

A.若甲为C,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化 3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
加酸歧化 3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
完成下列填空:
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和______________。(填序号)
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.泥三角
(2)在“加酸岐化”时不宜用硫酸的原因是__________;不宜用盐酸的原因是____________。反应之后得到高锰酸钾的步骤是:过滤、蒸发结晶、趁热过滤。该步骤能够得到高锰酸钾的原理是____________。
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O![]() 2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为_________________。
2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为_________________。
(4)草酸钠滴定法测定高锰酸钾的质量分数步骤如下:
已知涉及到的反应:
Na2C2O4+H2SO4=H2C2O4(草酸)+Na2SO4 ,
5H2C2O4+ 2MnO4—+6H+=2Mn2++10CO2↑+ 8H2O
Na2C2O4的式量:134 KMnO4的式量:158)
Ⅰ.称取0.80 g 的高锰酸钾产品,配成50mL溶液。
Ⅱ.称取0.2014 gNa2C2O4,置于锥形瓶中,加入蒸馏水使其溶解,再加入少量硫酸酸化。
Ⅲ.将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点。消耗高锰酸钾溶液8.48mL。
a.判断达到滴定终点的标志是____________________________。
b.样品中高锰酸钾的质量分数为______________(保留3位小数)。
c.加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度__________。(填“偏高”、“偏低”或“无影响”)
d.将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应溶液中Mn2+的浓度随反应时间t的变化如图,其原因可能为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )

A.H2SO4浓度为4mol/L
B.溶液中最终溶质为FeSO4
C.原混合酸中NO3﹣浓度为0.2mol/L
D.AB段反应为:Fe+2Fe3+→3Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用稀HNO3和Cu制取少量NO并验证氮氧化合物性质的装置.下列说法错误的是( )

A.吸收剂可以是NaOH溶液B.试管上部的气体始终为无色
C.小试管中溶液最终呈蓝色D.试纸先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向两支盛有2 mL相同浓度银氨溶液的试管中滴加2滴相同浓度的NaCl和NaI溶液 | 一支产生黄色沉淀,另一只无明显现象 | Ksp(AgI)<Ksp(AgCl) |
B | 向10 mL 0.1 mol/L AgNO3溶液中滴加2滴0.01 mol/L NaBr溶液,再滴加2滴0.01 mol/ LNa2S溶液 | 先产生浅黄色沉淀,然后出现黑色沉淀 | Ksp(AgBr)>Ksp(Ag2S) |
C | 向盛有2 mL 0.1 mol/L MgCl2溶液的试管中先滴加2滴2 mol/L NaOH溶液,再滴加2滴0.01 mol/L CuCl2溶液 | 先产生白色沉淀,然后白色沉淀变蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
D | 将H2S通人浓度均为0.01 mol/L的ZnSO4和CuSO4混合液中 | 先产生黑色的CuS沉淀 | Ksp(ZnS)>Ksp(CuS) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生氢材料甲由X、Y两种元素组成,两元素的原子最外层电子数相等。为确定甲的组成,进行了如下实验:
①称取1.2g甲固体与一定量的水蒸气刚好完全反应,生成标准状况下1.12L可燃性单质气体乙,同时得到2g化合物丙。
②用0.05mol甲与0.8g氧气恰好发生化合反应,得到2g丙。
请回答:
(1)乙的分子式____。
(2)写出甲与氧气反应生成丙的化学方程式____。
(3)设计实验方案检验丙中的阴离子_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com