
【题目】化学家借助太阳能产生的电能和热能,用空气和水作原料合成了氨气.下列有关说法正确的是( )
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
科目:高中化学 来源: 题型:
【题目】下列中和反应对应的离子方程式能以“H++OH-═H2O”表示的是
A.醋酸和氢氧化钠溶液反应B.氢氧化镁和盐酸反应
C.澄清石灰水和硝酸反应D.氢氧化钡和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关微粒的说法正确的是( )
A.分子可以再分,而原子不能再分B.分子、原子、离子都可以构成物质
C.原子失去电子变成阴离子D.分子大,原子小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】属于氧化还原反应的离子方程式的是( )
A.CaCO3+2H+= Ca2++CO2↑+H2OB.2Fe2++Cl2= 2Fe3++2Cl-
C.HCO3-+H+= CO2↑+H2OD.2Na+2H2O = 2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
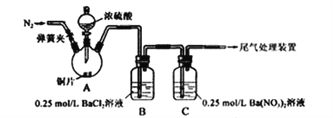
实验操作和现象:
操作 | 现象 |
关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(1)A中反应的化学方程式是_________________;
(2)C中生成白色沉淀的离子方程式为__________________;
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是_____________。
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2.4molA和1.2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应A(g)+B(g)xC(g)+D(g)△H<0,2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等;2min内v(B)=
(2)A的转化率为
(3)该反应的平衡常数的表达式k= , 450℃时平衡常数500℃时平衡常数(填“大于”、“小于”或“等于”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:
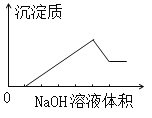
A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com