
| A、标准状况下,2.24L乙炔中含σ键数目为0.1 NA |
| B、常温常压下,1.6g O2所含氧原子数目为0.1NA |
| C、5.6g Fe和足量稀硝酸反应,转移电子数目为0.2NA |
| D、1L 0.1mol?L-1 Na2CO3溶液中含阴、阳离子总数目为0.3NA |


科目:高中化学 来源: 题型:
| A、均存在电离平衡和水解平衡 |
| B、存在的粒子种类相同 |
| C、c(OH-)前者大于后者 |
| D、分别加入NaOH固体,恢复到原温度,c(CO32-)、c(HCO3-)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中一定有离子键,没有共价键 |
| B、共价化合物中一定有共价键,没有离子键 |
| C、分子晶体中一定含有共价键 |
| D、非极性分子中不可能含有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 取代苯甲醛 | 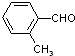 |  |  |  |
| 产率(%) | 15 | 23 | 33 | 0 |
| 取代苯甲醛 |  |  |  |  |
| 产率(%) | 71 | 63 | 52 | 82 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的质子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答:
如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的质子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com