
| A. | 在元素周期表金属与非金属分界线附近能找到制半导体材料的元素 | |
| B. | 离子键、共价键、氢键都是化学键 | |
| C. | 元素周期律是元素原子核外电子排布周期性变化的必然结果 | |
| D. | 元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑 |
分析 A、半导体材料的元素在元素周期表金属与非金属分界线附近能找到;
B、氢键是分子间作用力,不是化学键;
C、元素原子核外电子排布周期性变化的必然结果是元素周期律;
D、元素周期表是元素周期律的具体表现形式.
解答 解:A、半导体材料的元素在元素周期表金属与非金属分界线附近能找到,故A正确;
B、氢键是分子间作用力,不是化学键,故B错误;
C、元素原子核外电子排布周期性变化的必然结果是元素周期律,故C正确;
D、元素周期表是元素周期律的具体表现形式,揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一,故D正确;
故选B.
点评 本题考查结构性质位置关系应用,侧重对基础知识的巩固,元素周期律的实质及理解是解题关键,难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
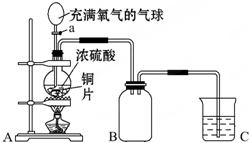 小明同学设计了如图所示装置来探究铜跟浓硫酸的反应.
小明同学设计了如图所示装置来探究铜跟浓硫酸的反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期元素中,Y的简单离子半径最小,且Y是地壳中含量最高的金属元素 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色的碱性溶液中:CrO42-、K+、Na+、SO42- | |
| B. | 使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量ClO-的溶液中:K+、H+、I-、SO42- | |
| D. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是一种核素 | B. | 原子核内有8个中子 | ||
| C. | 与${\;}_{6}^{12}$C互为同位素 | D. | 比${\;}_{6}^{13}$C少一个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com