
�Ȼ�����(S2Cl2)�ǹ㷺������ҵ����������ӽṹ����ͼ��ʾ��������S2Cl2��һ�ֳȻ�ɫ��Һ�壬��ˮ��ˮ�⣬��������ʹƷ����ɫ�����塣����˵��������ǣ� ��
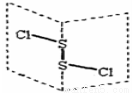
A��S2Cl2�ĽṹʽΪCl��S��S��Cl
B�� S2Cl2Ϊ���м��Լ��ͷǼ��Լ��ķǼ��Է���
C��S2Br2��S2Cl2�ṹ���ƣ��۷е㣺S2Br2>S2Cl2
D��S2Cl2��H2O��Ӧ�Ļ�ѧ����ʽ����Ϊ�� 2S2Cl2+2H2O=SO2��+3S��+4HCl
 С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ʡ������2017����������ε��в��Ի�ѧ�Ծ� ���ͣ�ѡ����
һ�����Ȼ����ȡ�����Ĺ���ԭ�����£�
��Ӧ��2NH4Cl+MgO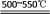 2NH3��+MgCl2+H2O��
2NH3��+MgCl2+H2O��
��Ӧ��2MgCl2+O2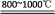 2MgO+2Cl2
2MgO+2Cl2
����˵����ȷ����
A. �ù�����MgO��ѭ������
B. ������ 1mol NH4Cl�Ƶ�Cl2�����һ��Ϊ11.2L
C. ��800~1000�������£�O2�Ļ�ԭ��ǿ��Cl2�Ļ�ԭ��
D. ����Ӧ2NH3+MgCl2+H2O��2NH4Cl+MgO���Է����У���÷�Ӧ��H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��У�����ڶ���������3�£����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʽΪC4H8O����Ԫ��ͬ���칹�干�У������������칹��( )
A. 5�� B. 6�� C. 7�� D. 8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����������и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ʯī�����Dz�״�ṹ����ÿһ���ڣ�ÿһ��̼ԭ�ڶ�������3��̼ԭ�����ϣ�����ͼ���侧��ṹ�ĸ���ͼ����ͼ��7����Ԫ����ȫռ�е�̼ԭ������
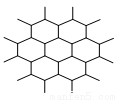
A.10�� B.18�� C.24�� D.14��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����������и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ij���Ӿ��徧������ͼ��ʾ����Ħ������ΪM�������ӵ�����ΪNA��������ܶ�Ϊd g/cm3������˵������ȷ����
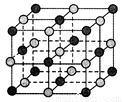
A. ���徧�������������ӵĸ�����Ϊ1
B. �þ������������������ͬ�����ӵĺ˼��Ϊ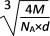 cm
cm
C. �������������ӵ���λ������4
D. �þ���������NaCl�ľ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и�һ3���¿���ѧ�Ծ��������棩 ���ͣ������
���в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
T | M���ϵĵ�������ԭ�Ӻ�����Ӳ�����2�� |
X | �����������Ǵ�����������2�� |
Y | �����µ��� |
Z | Ԫ����������ǣ�7�� |
(1)Y�γɵ�˫ԭ�ӷ����еĻ�ѧ��Ϊ_____________������Լ����Ǽ��Լ�������
(2)Ԫ��X��һ��ͬλ�ؿɲⶨ�������������ͬλ�صķ�����________��
(3)Ԫ��Y����Ԫ���γ�һ�ַ���YH3��д�������ӵĵ���ʽ��________��
(4)Ԫ��Z��Ԫ��T��ȣ��ǽ����Խ�ǿ����__________(��Ԫ�ط��ű�ʾ)�����б�������֤����һ��ʵ����________��
a��������Z�ĵ��ʺ�T�ĵ���״̬��ͬ
b��Z���⻯���T���⻯���ȶ�
c��һ��������Z��T�ĵ��ʶ���������������Һ��Ӧ
(5)T��X��Z����Ԫ�ص�����������ˮ�����������ǿ������˳����________________________(�û�ѧʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡĵ�����и�һ3���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��ZΪ������Ԫ�أ�ԭ��������������Xԭ��������������Yԭ��������������2������������Y��5��X��Z��ͬһ���塣������������ȷ���� ��������
A. ԭ�Ӱ뾶��Y��Z
B. XԪ�ص�һ�ֵ��ʿ���������ɱ��
C. Y�ĵ����ڿ����з��ñ��� ������һ�����ܵ�����Ĥ
������һ�����ܵ�����Ĥ
D. Z�ĵ����������е�ȼ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ������������������ۻ�ѧ�Ծ��������棩 ���ͣ������
��.�ߴ���������þ�㷺Ӧ����ҽҩ������������þ�����ο�ʯ����������������þ����Ҫ����������ͼ��ʾ��
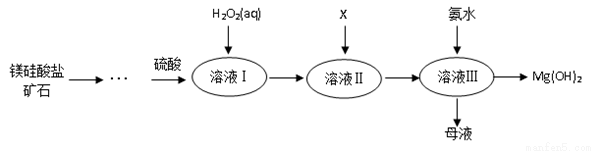
��֪��
����Һ���г���Mg2+��SO42?�⣬����������Fe3+��Al3+��Fe2+�����ӣ�
�ڳ����£����ֽ������ӿ�ʼ�����ͳ�����ȫʱ��pH���±���ʾ��
�������� | Fe3+ | Al3+ | Fe2+ | Mg2+ |
��ʼ����ʱ��pH | 1.5 | 3.3 | 6.5 | 9.4 |
������ȫʱ��pH | 3.7 | 5.2 | 9.7 | 12.4 |
��ش��������⣺
��1��þ��Ԫ�����ڱ��е�λ��_______________��
��2������Һ���м����Լ�X��_____________��������_________________________��
��3�������в���H2O2����ĺ����___________________________________��
��4��˵��ĸҺ��һ����;___________________��
��5������H2O2��Һ������Ӧ�����ӷ���ʽ��___________________��
��.��ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽����
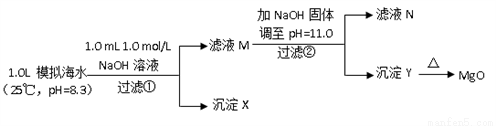
ģ�⺣ˮ�е�����Ũ��/ ��mol/L�� | Na+ | Mg2+ | Ca2+ | Cl�� | HCO3�� |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol/L������Ϊ�����Ӳ����ڣ�ʵ������У�������Һ������䡣
��֪��Ksp(CaCO3)��4.96��10��9��Ksp(MgCO3)��6.82��10��6��Ksp [Ca(OH)2]��4.68��10��6��Ksp [Mg(OH)2]��5.61��10��12����ش��������⣺
��6��������XΪ_____________��
��7����ҺN��Ca2��Ũ��Ϊ_______________��
��8����NaO H�������pH=12.5�Ƿ����______����ǡ�������ԭ����________��
H�������pH=12.5�Ƿ����______����ǡ�������ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ̫ԭ�и���ģ�⿼�ԣ�һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ҹ���ѧ������Ȼ�������о�����ȡ�����½�չ��������ͼװ�ÿɷ�����Ӧ��H2S+O2=H2O2+S����֪�׳��з����ķ�Ӧ��
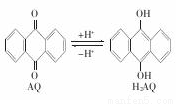
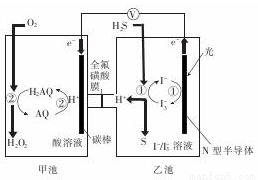
����˵����ȷ���ǣ� ��
A. �׳���̼���Ϸ����ĵ缫��ӦΪAQ+2H+-2e-=H2AQ
B. �ҳ���Һ�з����ķ�ӦΪH2S+I3-=3I-+S+2H+
C. ��װ���е���ת��Ϊ����
D. H+�Ӽ׳������ҳ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com