
(1)在CH4、H2S、NH4+、H2O、OH—、HCl、Na、Mg2+八种粒子中,选择符合下列要求的粒子填空:
①上述粒子中与K+质子数不同,电子数相同的有 ;
②上述粒子中与NH3质子数相同,电子数也相同的有 ;
③上述粒子中电子数大于质子数的有 。
(2)用锌片、铜片和稀硫酸组成的原电池,该电池的负极材料是 ,正极的电极反应式为 ,电池工作时电子流向 (填“正极”或“负极”)。
(3)将6molA气体和2molB气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g) xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
①x的数值为 ;
②A的平均反应速率为 ;
③5min时B的转化率为 。
(13分)(1) ①H2S、HCl (1分) ②CH4、H2O (1分) ③OH— (1分)
(2) 锌片 (1分) 2H++2e—=H2↑ (2分) 正极 (1分)
(3)① 1 (2分) ②0.3mol?L-1?min -1(2分) ③50% (2分)
【解析】
试题分析:(1)①K+质子数于电子数分别是19和13,则与K+质子数不同,电子数相同的有H2S、HCl。
②氨气含有10个质子和10个电子,则与NH3质子数相同,电子数也相同的有CH4、H2O.
③电子数大于质子数,说明带负电荷,则是OH-。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,据此可知,该电池的负极材料是锌片,铜是正极,溶液中的氢离子得到电子,则正极的电极反应式为2H++2e—=H2↑,电池工作时电子流向正极。
(3)①经5min后反应达到平衡状态,容器内的压强变小,这说明该反应是体积减小的可逆反应,即3+1>x+2,所以x只能是1;
②D的平均反应速率为0.2mol/(L?min),则根据反应速率之比是相应的化学计量数之比可知,A的平均反应速率是0.3mol/(L?min)。
③生成D的物质的量是0.2mol/(L?min)×5min×2L=2mol,所以消耗B的物质的量是1mol,则B的转化率是50%。
考点:考查质子数和电子数的计算、原电池的判断以及反应速率的有关计算等
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和训练,旨在培养学生灵活运用基础知识解决实际问题的能力,难度不大,有利于培养学生的规范答题能力,提高学生的应试能力。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
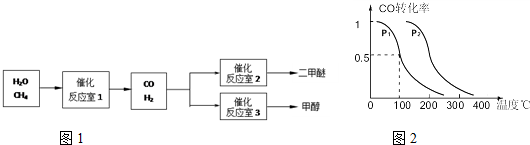
查看答案和解析>>
科目:高中化学 来源: 题型:

| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 此题分A、B题,任选一题答题,两题都做分数以A题为准,B题较容易.
此题分A、B题,任选一题答题,两题都做分数以A题为准,B题较容易.| 乙醇与钠反应的现象 | 气体燃烧的现象 | 检验产物 |
| ① Na沉到试管底部 Na沉到试管底部 ② 反应有气泡产生 反应有气泡产生 ③ 反应时放出热量 反应时放出热量 |
蓝色 蓝色 有水珠(或有水雾) 有水珠(或有水雾) 不变浑浊 不变浑浊 |
H2 H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com