
| A. | 0.43 | B. | 0.47 | C. | 0.49 | D. | 0.52 |
分析 先计算完全燃烧0.453mol碳需要的空气的量,再计算所需空气中含有的氮气的量,同时有0.453molCO2生成,还有1molCaCO3完全分解产生的气体,进行解答本题.
解答 解:完全燃烧0.453mol碳需要消耗0.453mol氧气(按空气中O2体积分数为0.21)计算,
则至少要空气的量为$\frac{0.453}{0.21}$=2.157摩尔,
其中含氮气的量为:2.157×0.79=1.704摩尔;
C+O2$\frac{\underline{\;点燃\;}}{\;}$ CO2,CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2 ↑,
1 1 1 1
0.453 x 1 y
由反应方程式可知:完全燃烧0.453mol碳生成 x=0.453mol 二氧化碳;
1mol碳酸钙分解生成y=1mol二氧化碳;
石灰窑产生的气体中CO2的体积分数=$\frac{1+0.453}{1+0.453+1.704}$×100%=45.9%≈46%;
这是最大值,如部分生成CO,则二氧化碳体积分数变小;
故选A.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
| 族 周期 | |||||||
| ① | |||||||
| Li | C | ④ | ⑤ | ⑥ | |||
| ⑦ | ⑧ | ⑨ | ⑩ | ||||
| K | ⑫ | ⑬ | |||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
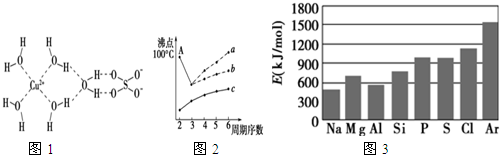
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
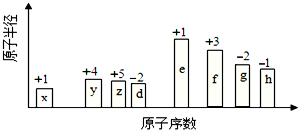 随原子序数的递增的八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.
随原子序数的递增的八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.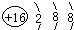 .
.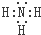 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
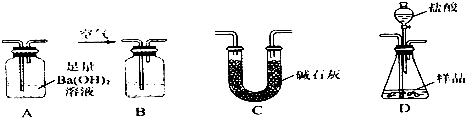
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品中大量添加苯甲酸钠等防腐剂,可以有效延长其保持期 | |
| B. | 利用丁达尔效应可区分淀粉溶液和NaCl溶液 | |
| C. | 明矾能水解生成Al(OH)3胶体,可用作饮用水消毒杀菌 | |
| D. | 石油分馏属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液:Na+、K+、SO42-、MnO4- | |
| B. | pH=1的溶液中:Fe2+、SO42-、Cl-、NO3- | |
| C. | 使酚酞变红的溶液:Na+、Cl-、SO42-、Fe3+、 | |
| D. | 水电离出的c(H+)=1×10-12mol/L的溶液:K+、Cl-、Ba2+、Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com