
【题目】一定温度下,某容器内发生反应N2(g)+3H2(g)![]() 2NH3(g),达到平衡的标志是
2NH3(g),达到平衡的标志是
A. 氨气、氮气、氢气的浓度相等B. 氮气和氢气的物质的量之比为1∶3
C. 氨气、氮气、氢气的浓度不变D. 恒温恒容时,混合气体的密度保持不变
科目:高中化学 来源: 题型:
【题目】在下列条件下,两种气体的分子数一定相等的是
A. 同密度、同压强的 N2 和 C2H4 B. 同温度、同体积的 O2 和 N2
C. 同体积、同密度的 C2H4 和 CO D. 同压强、同体积的 O2 和 N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一小块钠放在坩埚里加热,下列实验现象正确的是( )
①金属先熔化 ②在空气中燃烧,火焰呈黄色 ③燃烧时火星四射
④燃烧后生成淡黄色固体 ⑤燃烧后生成白色固体
A. ①②③ B. ①②④ C. ①②⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,改变反应物中n(SO2)对反应2SO2(g)+O2(g) 2SO3(g) △H<0的影响如图所示,下列说法正确的是
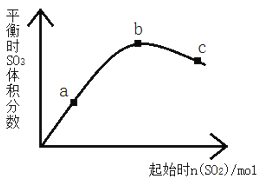
A. 反应b、c点均为平衡点,a点未达平衡且向正反应方向进行
B. a、b、c三点中,a点时SO2的转化率最高
C. 反应a、b、c点均为平衡点,b点时SO2的转化率最高
D. a、b、c三点的平衡常数Kb>Kc>Ka
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液显中性,金属离子已完全沉淀,沉淀质量为39.2g,求(写出计算过程):
(1)原固体混合物中Cu和Cu2O的物质的量之比为_____________;
(2)产生的NO在标准状况下的体积是________毫升?
(3)硝酸的物质的量浓度是________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H1=-159.47kJ/mol K1
NH2COONH4(s) △H1=-159.47kJ/mol K1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3 K3
CO(NH2)2(s)+H2O(g) △H3 K3
请回答:
(1)①总反应的△H3=_______kJ/mol。该热化学方程式的平衡常数K3=______(用K1、K2表示)。
②一定温度下,在体积固定的密闭容器中按计量比进行反应I,下列不能说明反应达平衡状态的是_____________。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2)
D.容器内混合气体的密度不再变化
③环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)。
(2)在体积可变的恒压 (P总) 密闭容器中充入1 mol CO2 与足量的碳,让其发生反应:C(s)+ CO2(g)![]() 2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。

①T℃时,达平衡后向容器中若充入稀有气体,v(正)___v(逆) (填“>”“<”或“=”);若充入等体积的CO2 和CO,平衡________移动(填“正向”“逆向”或“不”)。
②650℃,CO2 的转化率为_____________。
③已知:气体分压(P分)=气体总压×体积分数。用平衡分压代替平衡浓度表示平衡常数,925℃时,Kp=_____________ (用含P总的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g) +2H2(g) ![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
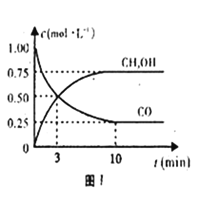
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入5mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况.反应第10分钟达到平衡,从反应开始到平衡,用H2表示平均反应速率v(H2)=______。
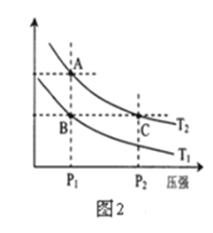
(2)图2表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A______C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A______C,由状态B到状态A,可采用______的方法(填“升温”或“降温”)。
(3)恒容条件下,下列措施中能使![]() 减小的有______
减小的有______
A.升高温度 B.充入He气 C.再充入2molCO和5molH2 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为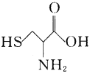 ,下列关于半胱氨酸说法不正确的是
,下列关于半胱氨酸说法不正确的是
A. 能溶于水、乙醇等溶剂
B. 既能与盐酸、又能与NaOH溶液反应
C. 与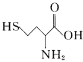 (高半胱氨酸)互为同系物
(高半胱氨酸)互为同系物
D. 官能团不变的同分异构体有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com