
����Ŀ����ͼ��Ԫ�����ڱ���һ���֣����еĢ�~����Ԫ�أ���ջش�
�� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
�� | �� | �� | �� | �� | ||||
�� | �� | �� | �� | �� | �� | �� |
��Ԫ�ط�������ѧʽ�ش��������⣺
��1������ЩԪ���У���ѧ��������õ�ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ______________��
��2����������ǿ�ĵ�����_____________��
��3����ЩԪ���е�����������Ӧ��ˮ�����У�������ǿ����_____________��������ǿ����_____________�������Ե�����������_____________��
��4��д���٢ڢۢ߶�Ӧ���⻯����ȶ�����ǿ��������_____________��
���𰸡�![]() F2 HClO4 NaOH Al(OH)3 H2O>NH3>CH4>SiH4
F2 HClO4 NaOH Al(OH)3 H2O>NH3>CH4>SiH4
��������
��Ԫ�����ڱ��е�λ�ÿ�֪����ΪCԪ�أ���ΪNԪ�أ���ΪOԪ�أ���ΪFԪ�أ���ΪNaԪ�أ���ΪAlԪ�أ���ΪSiԪ�أ���ΪSԪ�أ���ΪClԪ�أ���ΪArԪ�أ��ݴ˷���������⡣
(1)����ЩԪ���У���ѧ��������õ�ԭ����Ar����ԭ�ӽṹʾ��ͼ�� ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(2)Ԫ�����ڱ��У�ͬһ���ڴ�������������������ǿ��ͬһ��������������������μ�����������Ԫ������������ǿ��Ԫ����F���䵥��ΪF2���ʴ�Ϊ��F2��
(3)Ԫ�����ڱ��У�ͬһ���ڴ������ҷǽ�����������ǿ�����������μ�����ͬһ����������·ǽ��������μ�����������������ǿ���ǽ�����Խǿ������������Ӧˮ���������Խǿ��������Խǿ������������Ӧˮ����ļ���Խǿ������F�����ۣ���������ǿ����HClO4��������ǿ����NaOH���������Ե���Al(OH)3���ʴ�Ϊ��HClO4��NaOH��Al(OH)3��
(4)�٢ڢۢ߷ֱ�ΪC��N��O��SiԪ�أ��ǽ�����Խǿ����̬�⻯��Խ�ȶ������ڷǽ����ԣ�O>N>C>Si�������̬�⻯����ȶ��ԣ�H2O>NH3>CH4>SiH4���ʴ�Ϊ��H2O>NH3>CH4>SiH4��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��PbCO3���������ᡢ�մɺͲ����ȹ�ҵ���ɷ�Ǧ��(��Ҫ�ɷ�ΪPbS����������FeS��)�����̿�(��Ҫ�ɷ�ΪMnO2)�Ʊ�PbCO3���������£�

��֪��PbCl2��������ˮ���Ҵ�����������ˮ�������ʵ��ܶȻ����±����Իش��������⣺
���� | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | PbCl2 | PbS | PbCO3 |
Ksp | 2��10-13 | 8.0��10-16 | 1��10-38 | 1.6��10-5 | 8.0��10-28 | 7.4��10-14 |
(1)PbCO3��������________��
(2)�������MnO2��������________��������ͼ�����ٵ���ѷ�Ӧ������________��

(3)����ڳ��ȳ��˵�ԭ����___________________��
(4)�����ϴ���õ��Լ���____________��
(5)����ҺY���ữ��Ȼ�����MnO2����Ӧ�����ӷ���ʽΪ__________������Ӧ��c(Mn2+)=0.2mol/L����һ��������Һ��pH�ɷ���Fe3+��Mn2+����Һ������pH��ΧΪ_______[c(Fe3+)��1��10-5 mol/Lʱ��ʾFe3+�ѳ�����ȫ]��
(6)����ܷ�Ӧ�����ӷ���ʽΪ______________��
(7)��ƷPbCO3��������PbCl2���ʣ��ᴿ��ʵ�鷽����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ʵ����
A.���ʵ���Ũ����ͬ�����������Һ�ʹ������Һ�У���������е�笠��������ʵ���Ũ�Ƚ�С
B.��10mL 0.1 mol/L��AgNO3��Һ�м���6mL��Ũ�ȵ�NaCl��Һ���а�ɫ�����������ټ���6 mL��Ũ�ȵ�Na2S��Һ����Һ�����к�ɫ�������ɣ�˵��Ksp��Ag2S��< Ksp��AgCl��
C.���ʵ���Ũ�Ⱦ�Ϊ0.02 mol/L������HX������NaX�������Ϻ�c(X��)+ c(HX)=" 0.02" mol/L
D.��֪Ksp��AgCl��=1.56��10-10��Ksp��Ag2CrO4��=9.0��10-12���ں�C1����CrO42��Ũ����ͬ����Һ�еμ�AgNO3��Һʱ����������Ag2CrO4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A+B=3C+4D�ķ�Ӧ��,���б�ʾ�÷�Ӧ�Ļ�ѧ��Ӧ�ٶ�������
A.V(A)=0.5mol/(L��s)B.V(B)=0.3mol/(L��s)
C.V(C)=0.8mol/(L��s)D.V(D)=1mol/(L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɵ����ϳɰ����ķ��������1918��ŵ������ѧ��������һ�ܱ������г���1molN2��3molH2����һ�������·�����ӦN2��3H2![]() 2NH3�������й�˵����ȷ���ǣ�
2NH3�������й�˵����ȷ���ǣ�
A.�ﵽ��ѧƽ��ʱ��N2����ȫת��ΪNH3
B.�ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯
C.�ﵽ��ѧƽ��ʱ����Ӧ��ֹͣ����
D.�ﵽ��ѧƽ��ʱ��N2��H2�������ʱ�Ϊ3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ���ԭ���ķ����Ǵ��ܺ��ܼ����ľ�������ǻ�ѧ�������һ���ش��ס�
��1����������������Ӧ��A��NaOH+HCl=NaCl+H2O��B��Zn+H2SO4=ZnSO4+H2�����ж��ܷ���Ƴ�ԭ���A��_____________��B��_____________������ܡ����ܡ���
��2������пƬ�ʹ�ͭƬͼ��ʽ����100mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬�ش��������⣺

������˵����ȷ����_______________��
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ��
B������ͭƬ��û�����Ա仯
C������ͭƬ�������١�����пƬ��������
D�����ձ�����Һ��pH������
������ͬʱ���ڣ����ձ��в������ݵ��ٶȣ���______________�ң��������������������
����д��ͼ�й���ԭ��صĸ����缫��Ӧʽ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ע�����м�������Na2SO3���壬����������Ũ����(�Բ��Ӵ�ֽ��Ϊ)���������й�˵����ȷ���ǣ� ��
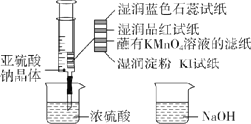
A.��ɫʯ����ֽ�ȱ�����ɫ
B.NaOH��Һ�����ڳ�ȥʵ���ж����SO2
C.ʪ�����-KI��ֽδ����˵��SO2��������ǿ��I2
D.Ʒ����ֽ��պ��KMnO4��Һ����ֽ��ɫ��������SO2��Ư����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�¶���CH3COOH��NH3��H2O�ĵ��볣����ȣ�����10 mLŨ��Ϊ0.1 mol��L��1��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ���ڵμӹ�����(����)
A. ˮ�ĵ���̶�ʼ������
B. c(NH4+)/c(NH3��H2O)�������ټ�С
C. c(CH3COOH)��c(CH3COO��)֮��ʼ�ձ��ֲ���
D. �����백ˮ�����Ϊ10 mLʱ��c(NH4+)��c(CH3COO��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶�����Һ������Զ�TiO2���ȼ��R���ⷴӦ��Ӱ����ͼ��ʾ�������жϲ���ȷ���ǣ� ��

A. �Ա�pH=7��pH=10�����ߣ���ͬһʱ�̣���˵��R����ʼŨ��Խ��������Խ��
B. �Ա�pH=2��pH=7�����ߣ�˵����Һ����Խǿ��R�Ľ�������Խ��
C. ��0~20min֮�䣬pH=2ʱR��ƽ����������Ϊ0.0875��10-4mol��L-1��min-1
D. 50minʱ��pH=2��pH=7ʱR�Ľ���ٷ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com