
【题目】下列说法错误的是
A. 抗酸药能中和胃里过多的盐酸,缓解胃部不适 ,是一类治疗胃痛的药
B. 碳酸镁、碳酸钡都能制成抗酸药
C. 青霉素有阻止多种细菌生长的优异功能,虽经1×107倍稀释,仍有疗效
D. 青霉素是重要的消炎药
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】工业上常常会大量的废料,如果不加以回收利用甚至会造成环境污染,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

请回答:
(1)写出步骤Ⅰ反应的离子方程式:_________________________。
(2)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是____________。
(3)进行步骤Ⅱ时,该小组用如图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是____________________。

(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径②中反应的离子方程式:__________________________,
请选出你认为的最佳途径并说明选择的理由:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是( )
A. 纯碱溶液滴入酚酞变红
B. 铁在潮湿的环境下生锈
C. 加热氯化铁溶液颜色变深
D. 用氯化铵溶液除去铁锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧气可发生如下反应:P4+5O2 == P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )

A.(6a+5d-4c-12b)kJ·mol-1 B.(4c+12b-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1 D.(4a+5d-4c-12b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系![]() ,下列有关物质的推断不正确的是
,下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2 B.若甲为Fe,则丁可能是盐酸
C.若甲为SO2,则丁可能是氨水 D.若甲为NaOH 溶液,则丁可能是H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5kJ·mol﹣1,ΔH2=-395.4kJ·mol﹣1,下列说法或表示式正确的是( )
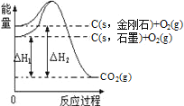
A.C(s,石墨)=C(s,金刚石) ΔH=-1.9 kJ·mol﹣1
B.石墨和金刚石的转化是物理变化
C.石墨的稳定性强于金刚石
D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程,属于放热反应的是( )
①工业合成氨 ②酸碱中和反应 ③水蒸气变成液态水 ④固体NaOH溶于水 ⑤Na在Cl2中燃烧 ⑥食物腐败 ⑦浓H2SO4稀释
A. ①②③④⑤⑥⑦ B. ②③④⑤ C. ①②⑤⑥ D. ①②⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢、氧两种元素组成的常见物质有H2O和H2O2,二者在一定条件下均可分解。
(1)已知:
化学键 | 断开1mol化学键所需的能量(kJ) |
H-H | 436 |
O-H | 463 |
O=O | 498 |
①H2O的电子式是________________。
②H2O(g)分解的热化学方程式是________________________。
③11.2 L(标准状况)的H2完全燃烧,生成气态水,放出__________kJ的热量。
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响。常温下,按照如表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 | |
a | 50 mL5%H2O2溶液 | 1 mL0.1 mol·L-1FeCl3溶液 | |
b | 50 mL5%H2O2溶液 | 少量浓盐酸 | 1 mL0.1 mol·L-1FeCl3溶液 |
c | 50 mL5%H2O2溶液 | 少量浓NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
d | 50 mL5%H2O2溶液 | MnO2 | |
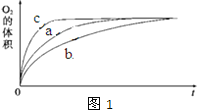
① 测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示。由该图能够得出的实验结论是______________________。
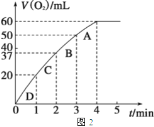
② 测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示。解释反应速率变化的原因________________;计算H2O2的初始物质的量浓度为________________ (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】刚刚从农业学院毕业的小刘,准备利用所学的知识在农村搞无土栽培。他配制的培养液中含有Mg2+、K+、Ca2+、Zn2+,其浓度都是0.1molL﹣1,培养一段时间后,培养液中剩余最多的是( )
A. Ca2+ B. Mg2+ C. K+ D. Zn2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com