
【题目】下列有关非金属元素说法正确的是
A.二氧化氯具有还原性,可用于自来水的杀菌消毒
B.液氨汽化时要吸收大量的热,可用作制冷剂
C.硫具有还原性,可用硫粉覆盖地上洒落的汞
D.硅是重要的半导体材料,常用于制作光导纤维
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】4P(红磷s)![]() P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
A. 正反应是一个放热反应
B. 当lmol白磷完全转变成红磷时放出17kJ热量
C. 当4g红磷转变成白磷时吸收17kJ热量
D. 白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某KCl样品中含有少量K2CO3、K2SO4和不溶于水的杂质。为了提纯KCl,先将样品溶于适量水中,搅拌、过滤,再将滤液按下图所示步骤进行提纯(过滤操作已略去)。下列说法正确的是

A.起始滤液常温下pH=7 B.试剂Ⅰ为Ba(NO3)2溶液
C.上图过程须经2次过滤 D.步骤③目的是除去CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B. 0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA
C. 反应3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
D. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某实验小组用如图所示的实验装置验证S、C、Si三种元素的非金属性强弱。
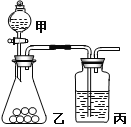
(1)仪器甲的名称为 ,甲中所盛试剂的化学式为 。
(2)乙中盛有白色粉末,可观察到的现象为 。
(3)丙中发生反应的离子方程式为 。
II.另一实验小组用该套装置验证氧化性 KMnO4>Cl2>I2 (已知高锰酸钾常温下可氧化浓盐酸生成氯气)。
(4)写出乙中发生反应的离子方程式: 。
(5)丙中盛有KI溶液和苯的混合物,丙中观察到的现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 同周期元素的原子半径以ⅦA族的为最大
B. 在周期表中0族元素的单质全部是气体
C. ⅠA、ⅡA族元素的原子,其半径越大越容易失去电子,第一电离能越大
D. 所有主族元素的原子形成单核离子时的价数都和它的族数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于浓硝酸和浓硫酸的叙述,正确的是
A.常温下都能用铝制容器贮存
B.露置在空气中,容器内酸液的质量都减轻
C.常温下都能与铜较快地反应
D.露置在空气中,容器内溶质的浓度都升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com