
【题目】下列叙述正确的是( )
A. 同周期元素的原子半径以ⅦA族的为最大
B. 在周期表中0族元素的单质全部是气体
C. ⅠA、ⅡA族元素的原子,其半径越大越容易失去电子,第一电离能越大
D. 所有主族元素的原子形成单核离子时的价数都和它的族数相等
科目:高中化学 来源: 题型:
【题目】
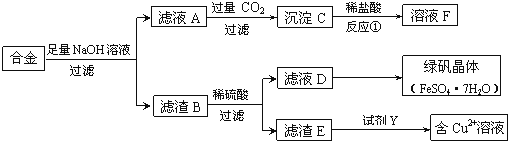
(1)合金与足量氢氧化钠溶液反应的离子方程式是 。
(2)若D中含有Fe3+,除去Fe3+的常用试剂是 。
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、过滤、自然干燥。
(4)若由滤渣E得到含Cu2+的溶液,试剂Y可能是 (填选项字母)。
A.稀硝酸 | B.浓硫酸 | C.浓盐酸 | D.稀硫酸 |
根据所选试剂写出一个由滤渣E得到含Cu2+溶液的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份,能使溴水褪色;A是一种重要的化工原料,它的产量通常用来衡量一个国家石油化工水平.现以A为主要原料合成乙酸乙酯及高分子化合物E,其合成路线如图所示:

请回答下列问题:
(1)写出A的电子式 .
(2)B、D分子中的官能团名称分别是 、 .
(3)写出下列反应的化学方程式并指出反应类型:
① 反应类型 ;
② 反应类型 ;
④ 反应类型 。
⑤ 反应类型 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关非金属元素说法正确的是
A.二氧化氯具有还原性,可用于自来水的杀菌消毒
B.液氨汽化时要吸收大量的热,可用作制冷剂
C.硫具有还原性,可用硫粉覆盖地上洒落的汞
D.硅是重要的半导体材料,常用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3NA
B.25℃时,pH=13的1.0 LBa(0H)2溶液中含有的OH-数目为0.2NA
C.常温常压下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA
D.1L1 mol·L-1FeCl3完全水解生成NA个胶体粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程的一部分:
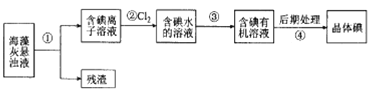
下列判断正确的是( )
A.步骤①、③的操作分别是过滤、萃取分液
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤③中加人的有机溶剂是乙醇
D.步骡④的操作是过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
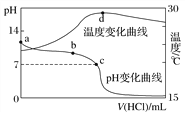
A. a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B. b点:c(NH![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)=c(NH![]() )
)
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com