
| A. | CO和N2 | B. | N2H4和 C2H4 | C. | CO2和N2O | D. | O3和SO2 |
分析 具有相同原子数和价电子数的微粒之间互称等电子体,等电子体往往具有相似的空间构型.
解答 解:A.CO和N2的原子个数都为2,价电子数:前者碳为4,氧为6,共为10,后者氮为5,2个氮原子共为10,原子数和价电子数都相等,属于等电子体,故A不符合;
B.N2H4 和C2H4的原子个数都为6,价电子数:前者氮为5,氢为1,共为14,后者碳为4,氢为1,共为12,原子数相等,但价电子数不相等,不属于等电子体,故B符合;
C.CO2和N2O的原子个数都为3,价电子数:前者碳为4,氧为6,共为16,后者氮为5,氧为6,共为16,原子数和价电子数都相等,属于等电子体,故C不符合;
D.O3和SO2的原子个数都为3,价电子数:前者氧为6,共为18,后者硫和氧都为6,共为18,原子数和价电子数都相等,属于等电子体,故D不符合;
故选B.
点评 本题考查了等电子体,解答本题关键是充分理解等电子体的本质特征,难度中等.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:推断题
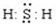
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥⑧ | B. | ①②④⑤⑥⑦⑧ | C. | ①③④⑤⑥⑦ | D. | ①④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖 | B. | 甘油 | C. | 氨基酸 | D. | 蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | HF | Ka=6.8×10-4 mol•L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol•L-1 |
| ③ | HCN | Ka=6.2×10-10 mol•L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol•L-1 Ka2=4.7×10-11 mol•L-1 |
 HCO3-+H+、HCO3-
HCO3-+H+、HCO3- CO32-+H+.
CO32-+H+.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com