
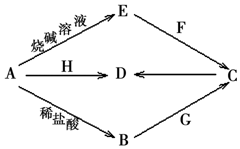
 短周期元素金属单质A可发生如图所示存在转化(部分反应物、反应条件和产物已略去).F是化石燃料燃烧产生的一种温室气体;常温下,G是一种有刺激性气味的气体,其水溶液显弱碱性;H是一种具有磁性的黑色氧化物;B、C、D、E四种化合物中含有一种相同的元素.
短周期元素金属单质A可发生如图所示存在转化(部分反应物、反应条件和产物已略去).F是化石燃料燃烧产生的一种温室气体;常温下,G是一种有刺激性气味的气体,其水溶液显弱碱性;H是一种具有磁性的黑色氧化物;B、C、D、E四种化合物中含有一种相同的元素.分析 F是化石燃料燃烧产生的一种温室气体,则F为二氧化碳气体;金属A能够与烧碱溶液、盐酸溶液反应,其中A与烧碱溶液生成的E溶液能够与二氧化碳反应,则A为Al;H是一种具有磁性的黑色氧化物,则H为Fe3O4;H能够与金属铝反应生成D,且B,C,D,E四种化合物中含有一种相同的元素,则D为氧化铝、C为氢氧化铝;B为氯化铝;气体G的水溶液为碱性,则G为氨气,以此解答该题.
解答 解:(1)由以上分析可知题目涉及Al(OH)3、Al2O3,为两性化合物,实验室制取氨气,通常采用氯化铵和氢氧化钙发生复分解反应,生成氯化钙、氨气和水制得氨气,化学反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,
故答案为:Al(OH)3、Al2O3;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
(2)金属铝与氢氧化钠溶液反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,该反应的实质为铝与水反应生成氢氧化铝和氢气,生成的氢氧化铝具有两性,能够与氢氧化钠溶液反应,从而使该反应能够发生,所以该反应中的氧化剂为H2O,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;H2O;
(3)A→D的化学方程式为3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,实验室中引发该反应的操作是加少量KClO3,插上镁条并将其点燃,
故答案为:3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3;加少量KClO3,插上镁条并将其点燃.
点评 本题考查了无机推断,为高频考点,题目难度中等,侧重考查铝及其化合物性质,明确常见金属及其化合物性质为解答关键,试题培养了学生的分析能力及灵活应用能力.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将少量硫酸铝溶液滴入氢氧化钠中 | 制备氢氧化铝 |
| B | 向碘化亚铁溶液中滴加酸化的双氧水 | 验证:氧化性H2O2>Fe3+ |
| C | 向CH2=CHCH2OH中滴加酸性重络酸钾溶液 | 证明有机物中含有羟基 |
| D | 室温下,测定0.1mol•L-1NaX、NaY溶液的pH | 探究HX、HY的电离常数大小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠保存在煤油或石蜡中 | |
| B. | 金属钠着火时,不能用泡沫灭火器来灭火 | |
| C. | 钠可以从水溶液中置换出活泼性排在其后面的金属 | |
| D. | 实验时用剩的钠块应该放回原试剂瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1molCCl4的体积约为22.4L | |
| B. | 0℃、101KPa时,2g氢气的体积约为22.4L | |
| C. | 通常状况下,22.4LCO2中所含分子数为NA个 | |
| D. | 1mol气体的体积只有在标准状况下才约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的NaClO溶液中含有ClO-的数目小于NA | |
| B. | Na2O2与足量CO2反应生成1molO2,转移的电子数目为2NA | |
| C. | 两份2.7g铝分别与100mL浓度为2mol•L-1的盐酸和氢氧化钠溶液充分反应,转移的电子数均为0.3NA | |
| D. | 18g重水(D2O)所含的电子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com