
| A. | 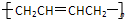 | B. |  | C. |  | D. |  |
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题
 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.| SO2Cl2 | Cl2 | SO2 | |
| 熔点 | -54.1 | -101 | -72.4 |
| 沸点 | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲降低温度,乙不变 | |
| B. | 甲中加入0.1molHe,乙不改变 | |
| C. | 甲、乙提高相同温度 | |
| D. | 甲增加0.1mol H2,乙增加0.1mol I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X是金属元素 | |
| B. | X的单质可作半导体材料 | |
| C. | X存在稳定的气态氢化物 | |
| D. | X最高价氧化物对应水化物的酸性较强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com