
| A、CuO→Cu |
| B、Fe→FeCl2 |
| C、HNO3→NO2 |
| D、Al2O3→NaAlO2 |
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
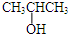 ⑨CH≡CH.
⑨CH≡CH.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某氨水的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a<b-1 |
| B、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
| C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 |
| D、若10mLpH=a的硫酸溶液跟100mLpH=b的NaOH溶液混合后,溶液呈中性,则a+b=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaCl(Na2CO3) | 盐酸 | - |
| B | CO2(CO) | O2 | 点燃 |
| C | Fe(Cu) | 稀硫酸 | 过滤 |
| D | CO2(HCl) | NaOH溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
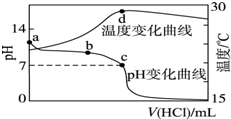 室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A、a点由水电离出的c(H+)<1.0×10-14mol/L |
| B、b点:n(NH4+)+n(NH3?H2O)>n(Cl-) |
| C、b点时加入的盐酸体积小于20.00mL,而c点时加入的盐酸体积大于20.00mL |
| D、d点后,温度略下降的主要原因是生成的NH4Cl水解吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,铝片可以溶解于足量浓硫酸,也可溶解于足量稀硫酸 |
| B、常温下,铜片与浓硝酸反应,不与稀硝酸反应 |
| C、常温下,浓的氢氧化钠溶液和极稀的氢氧化钠溶液均能溶解Al(OH)3 |
| D、加热条件下,MnO2能与浓盐酸反应生成氯气,与稀盐酸则不行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电池放电时的总反应为2Na+NiCl2═Ni+2NaCl |
| B、充电时阳极的电极反应为Na++e-═Na |
| C、放电时正极的电极反应为Ni2++2e-═Ni |
| D、该电池被称为绿色电池,最大原因是从废弃电池中可以方便地回收较纯的镍,其他产物对环境没有影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com