
下列关于有机物的说法错误的是
A.乙酸的分子式为CH3COOH,属于弱电解质
B.食醋中含有乙酸,乙酸可由乙醇氧化得到
C.乙醇中是否含有水,可用无水硫酸铜来检验
D.乙醇和乙酸的熔点和沸点都比C2H6、C2H4的熔点和沸点高
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届四川省高三入学考试化学试卷(解析版) 题型:选择题
在化学学科中经常使用下列物理量,其中跟阿伏加德罗常数(NA)无关的组合是 ( )
①相对原子质量 ②摩尔质量(g·mol-1) ③原子半径 ④中和热(kJ·mol-1)
⑤物质的量 ⑥化学反应速率[mol·L-1·s-1)] ⑦气体摩尔体积(L·mol-1) ⑧溶解度
⑨燃烧热(kJ·mol-1) ⑩溶质的质量分数
A.①③⑧⑩ B.②④⑤⑥⑦⑨ C.①②③④⑤ D.⑥⑦⑧⑨⑩
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市2012级临诊考试化学试卷(解析版) 题型:选择题
化学与生活宙哪相关,下列用选、性质或变化对应正确的是
A.利用粮食酿酒的化学过程包含:淀粉一→葡萄糖一→己醇
B.在月饼包装袋中放人生石灰:防止食物氧化变质
C.焰火的绚丽:说明只有金属单质能发生焰色反应
D.氢氧化铝用于清疗胃酸过多:氢氧化锯碱性强
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三8月开学测试化学试卷(解析版) 题型:填空题
(10分)Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:
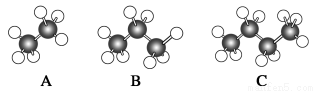
(1)A、B、C三者的关系是_________ ___。
(2)A的分子式为_____ _____,C的名称为______ ____。
(3)写出C的同分异构体的结构简式:________________________________。
Ⅱ.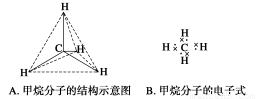
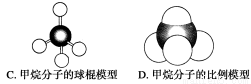
以上各图均能表示甲烷的分子结构,__________种更能反映其真实的存在状况。
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三8月开学测试化学试卷(解析版) 题型:选择题
有关分子结构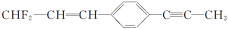 的下列叙述中,正确的是
的下列叙述中,正确的是
A.可能在同一平面上的原子最多有20个 B.12个碳原子不可能都在同一平面上
C.所有的原子都在同一平面上 D.除苯环外的其余碳原子有可能都在一条直线上
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三8月开学测试化学试卷(解析版) 题型:选择题
下列关于油脂的叙述中,不正确的是
A.油脂是酯的一种
B.植物油和矿物油都不能使溴水褪色
C.天然油脂没有固定的熔点和沸点,所以天然油脂是混合物
D.油脂在人体内的化学变化主要是在脂肪酶的催化下进行水解
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:填空题
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:___________________________
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确。试剂X是 。
A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 (填“甲”或“乙”)判断正确。
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH—浓度分别为amol /L和bmol /L,则a与b的比值= 。
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是( )
4NO(g)+ 6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源:2015届云南省云龙县高二下学期期末考试化学试卷(解析版) 题型:推断题
【化学选修2:化学与技术】(15分)工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:

已知:①NaHSO4溶解度随温度的升高而增大,适当 条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是 。
(2)反应器Ⅱ中发生反应的离子方程式为 。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是 。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有 ,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com