
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶性的甲基磺酸铅为电解质,电池总反应为:Pb +PbO2 + 4H+  2Pb2+ + 2H2O. 下列有关新型液流式铅酸蓄电池的说法正确的是( )
2Pb2+ + 2H2O. 下列有关新型液流式铅酸蓄电池的说法正确的是( )
A. 放电时负极反应式为Pb – 2e- + SO42- = PbSO4
B. 充放电时,溶液的导电能力变化不大
C. 以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L
D. 充电时的阳极反应式为Pb 2+ + 2e- + 4OH- = PbO2 +2H2O
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
闪电时空气中有臭氧生成。下列说法中正确的是
A.O3和O2互为同位素
B.O2比O3稳定
C.等体积O3和O2含有相同质子数
D.O3与O2的相互转变是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关微粒之间关系和特征描述正确的是( )。
| 选项 | 微粒 | 相互关系 | 特征描述 |
| A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
| B | 新戊烷、2,2-二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
| C |
| 同素异形体 | 铂作氨催化氧化时的催化剂 |
| D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
相对分子质量为M的气态化合物V L(标准状况),溶于m g水中,得到质量分数为w%的溶液,物质的量浓度为c mol/L,密度为ρ g·cm-3,则下列说法正确的是( )
A.相对分子质量M= B.物质的量浓度c=
B.物质的量浓度c=
C.溶液的质量分数w%=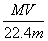 D.溶液密度ρ=
D.溶液密度ρ=
查看答案和解析>>
科目:高中化学 来源: 题型:
常温时,下列各组粒子在指定条件下,一定能大量共存的是( )
A. 水电离出c(H+) =10-13 mol / L 的溶液中 : Fe2+ NO3- k+ Cl-
B. 在NaAlO2溶液中:k+ CO32- SO42- S2-
C. 甲基橙呈红色溶液中: Na+ ClO- Al3+ NO3-
D. 含FeCl3 溶液中: Cl- k+ H2O2 NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有等物质的量的ZnSO4, Fe2(SO4)3, H2 SO4, CuSO4,向其中逐渐加入铁粉,溶液中Fe2+的物质的量(纵坐标/mol)和加入铁粉的物质的量(横坐标/mol)之间的关系为( )
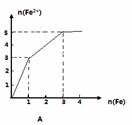
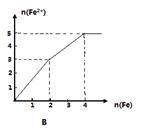

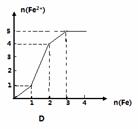
查看答案和解析>>
科目:高中化学 来源: 题型:
现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要 时可加热)能用于鉴别它们的是
时可加热)能用于鉴别它们的是
①观察颜色 ②石蕊试液 ③品红溶液
A.①②③ B.只有①③
C.只有②③ D.只有①②
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜,制备方法如下:
方法一:
(1)浓硫酸试剂瓶上适合贴上的标签是________(填序号)。

(2)甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分,设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:____________________________________________________。
实验结论:所得灰白色固体的化学式为________。
(3)乙还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是(用化学方程式回答)________________________________________________________________________。
直到最后反应完毕,发现试管中还有铜片剩余,乙根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是_____________________________________________。
方法二:
(4)丙同学认为甲设计的实验方案不好,他自己设计的思路是2Cu+O2 2CuO,CuO+H2SO4===CuSO4+H2O。
2CuO,CuO+H2SO4===CuSO4+H2O。
对比甲的方案,你认为丙同学的优点是①__________________________________;
②____________________________________________________________________。
方法三:
(5)丁同学取一铜片和稀硫酸放在试管中,再 向其中滴入双氧水发现溶液逐渐呈蓝色,写出反应的化学方程式__________________________________________________。
向其中滴入双氧水发现溶液逐渐呈蓝色,写出反应的化学方程式__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B 进行如下反应:3A(g)+2B(g)  4C(s)+2D(g),反应一段时间后达到平衡,测得生成
4C(s)+2D(g),反应一段时间后达到平衡,测得生成
1.6 mol C,则下列说法正确的是
A.该反应的化学平衡常数表达式是K=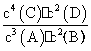 B.此时,B的转化率是40%
B.此时,B的转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加B,平衡向右移动,B的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com