
下列有关微粒之间关系和特征描述正确的是( )。
| 选项 | 微粒 | 相互关系 | 特征描述 |
| A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
| B | 新戊烷、2,2-二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
| C |
| 同素异形体 | 铂作氨催化氧化时的催化剂 |
| D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
等物质的量的下列化合物在相应条件下完全分解后得到氧气最多的是
A.KClO3(加MnO2催化剂,加热) B.KMnO4(加热)
C.H2O2(水溶液,加MnO2催化剂) D.HgO(加热)
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。(b)反应①、②是化工生产中的重要反应。(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。(e)化合物J由两种元素组成,其相对分子质量为32。
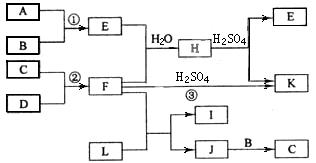
请按要求填空:
⑴反应③的化学方程式__________________________。
⑵C的结构式______________;H的化学式______________。
⑶L的溶液与化合物E反应的离子方程式__________________________。
⑷化合物J的化学式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近期,北京大学的两位教授率先发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用。下列叙述正确的是( )
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外电子层都达到8电子结构
C.将硫化氢通入溴水,溴水褪色
D.硫化氢是电解质,其电离方程式是H2S===2H++S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
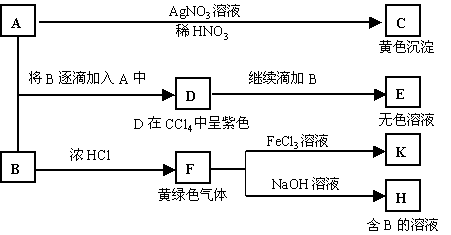
请回答:
(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
,
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5 mol/L,下面四个选项中能达到此目的的是( )
A.Fe2+、Na+、NO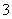 、Cl- B. Mg2+、NH
、Cl- B. Mg2+、NH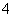 、SO
、SO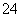 、NO
、NO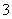
C.H+、K+、Cl-、CH3COO- D.Fe3+、K+、AlO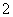 、SO
、SO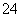
查看答案和解析>>
科目:高中化学 来源: 题型:
反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
2NaI+MnO2+3H2SO4===2NaHSO4+MnSO4+2H2O+I2(1)
2NaIO3+5NaHSO3===2Na2SO4+3NaHSO4+H2O+I2(2)下列说法正确的是 ( )
A.两个反应中NaHSO4均为氧化产物
B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物
C.氧化性:MnO2>SO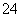 >IO
>IO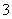 >I2
>I2
D.反应(1)、(2)中生成等量的I2时转移电子数比为1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶性的甲基磺酸铅为电解质,电池总反应为:Pb +PbO2 + 4H+  2Pb2+ + 2H2O. 下列有关新型液流式铅酸蓄电池的说法正确的是( )
2Pb2+ + 2H2O. 下列有关新型液流式铅酸蓄电池的说法正确的是( )
A. 放电时负极反应式为Pb – 2e- + SO42- = PbSO4
B. 充放电时,溶液的导电能力变化不大
C. 以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L
D. 充电时的阳极反应式为Pb 2+ + 2e- + 4OH- = PbO2 +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子
B.标准状况下,2.24 L水中含有6.02×1022个水分子
C.2.24 L氨气分子中含6.02×1023个电子
D.2.4 g金属镁变为镁离子时失去6.02×1022个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com