
【题目】下列说法正确的是( )
A.控制塑料购物袋的使用主要是为了节约成本
B.使用可降解塑料袋有利于减少“白色污染”
C.聚氯乙烯塑料袋可用来长时间存放食品
D.塑料购物袋具有热固性,不能回收利用
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】关于氧化还原反应的下列说法中正确的是( )
A.氧化还原反应前后元素化合价没有升降
B.氧化还原反应前后一定有氧的得失
C.氧化还原反应前后一定有电子转移
D.复分解反应和化合反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1L某混合溶液中可能含有的离子如下表:
可能大量含有的阳离子 | H+、NH4+ 、Al3+、K+ |
可能大量含有的阴离子 | Cl﹣、Br﹣、I﹣、ClO﹣、AlO2﹣ |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如图所示.
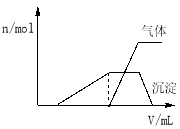
①则该溶液中确定含有的离子有 ;
②不能确定是否含有的阳离子有 ;
③要确定其存在可补充做的实验是 ;
④肯定不存在的阴离子有 .
(2)经检测,该溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
n(Cl﹣) | 1.25mol | 1.5mol | 2mol |
n(Br﹣) | 1.5mol | 1.4mol | 0.9mol |
n(I﹣) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为 .
②原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数,下列对于0.3mol/L的硫酸钾溶液的说法中不正确的是( )
A. 1L溶液中含有0.6NA个钾离子
B. 1L溶液中含有钾离子和硫酸根离子总数为0.9NA
C. 2L溶液中钾离子浓度为1.2mol/L
D. 2L溶液中含有硫酸根离子0.6NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列家庭小实验中不涉及化学变化的是( )
A.用熟苹果催熟青香蕉 B.用少量食醋除去水壶中的水垢
C.用糯米、酒曲和水制成甜酒酿 D.用木炭除去冰箱中的异味
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有0.1 mol·L-1 AlCl3和0.3 mol·L-1 NH4Cl的混合液1 L中加入0.1 mol·L-1 NaOH溶液 (纵坐标为沉淀的物质的量,横坐标为加入试剂的体积)正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50mol/LNaOH溶液
若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体___________g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。

取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
(1)写出该反应的热化学方程式为___________(中和热为57.3kJ/mol);
(2)①请填写下表中的空白:

②近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃)。则中和热△H=___________(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是___________(填字母)
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为生活中的常见金属,C为磁性黑色晶体,A、B、C、D之间转化关系

(1)写出以下物质的化学式A_________、C__________、D___________。
(2)C+盐酸→B+D的离子方程式为____________________________,D的溶液可作为
印刷电路板“腐蚀液”,写出该反应的化学方程式______________________。
(3)实验室保存B的溶液时常加入少量A,原因是_________________________(用
离子方程式表示)
(4)向B溶液中滴加NaOH溶液,产生的现象是___________________,过程中所发
生的氧化还原反应的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入润洗过的锥形瓶中,并加入1或2滴酚酞溶液
⑤滴入一滴标准液后,溶液颜色由无色变为红色立即停止滴定,记录液面读数
请回答:
(1)以上步骤有错误的是(填编号) 。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入_________中。(从图中选填“甲”或“乙”)

(3)下列操作会引起实验结果偏大的是:_________(填编号)
A.酸式滴定管未润洗
B.滴定前,滴定管尖嘴无气泡,滴定后有气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.滴定结束时仰视滴定管,并记录数据
E.滴定过程中有一滴标准液飞溅出锥形瓶
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视 。
II.利用中和滴定的原理,在工业生产中还可以进行氧化还原滴定测定物质含量。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉状TiO2。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(5)除去TiCl4含有的杂质A3+可选用调节pH的方法使其转化为A(OH)3沉淀除去。已知Al(OH)3的![]() ,若想将Al3+完全沉淀(不考虑钛离子的沉淀),则溶液的pH一定不能小于__________。(
,若想将Al3+完全沉淀(不考虑钛离子的沉淀),则溶液的pH一定不能小于__________。(![]() 时,即可认为完全沉淀)
时,即可认为完全沉淀)
(6)TiCl4水解生成TiO2·xH2O的化学方程式为__________________________。
(7)滴定终点的现象是___________________________。
(8)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com