
【题目】某强酸性溶液 X:可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,转化关系如图所示。反应过程中有一种气体在空气中会变为红棕色。回答下列问题:

(1)由题给信息可知,溶液X中确定不存在的阴离子有_______________。
(2)沉淀C是______ (填化学式),由此可确定溶液X中肯定不存在的阳离子有________。
(3)气体A是________(填化学式),产生气体A的离子方程式为________________。
(4)________ (填“能” 或“不能”)根据沉淀E确定溶液X中存在Fe3+,理由是________。
(5)步骤④中发生反应的离子方程式为________________。
(6)根据题给信息和图中转化关系,可以确定溶液X中肯定存在的离子有________,可能存在的离子有________。检验可能存在的离子是否存在的方法是________。
【答案】 CO32-、SiO32-、NO3- BaSO4 Ba2+ NO 3Fe2++4H++NO3-=3Fe3++NO↑+2H2O 不能 溶液B中含有由Fe2+氧化得到的Fe3+,故无法确定溶液X中是否存在Fe3+ AlO2-+CO2+2H2O=A l(OH)3↓+ HCO3- Al3+、NH4+、SO42-、Fe2+ Fe3+ 取少量溶液X于试管中,滴加几滴KSCN溶液,若溶液变红色,则溶液X中含有Fe3+;若溶液不变红色,则溶液X中不含有Fe3+
【解析】溶液显酸性,则一定不存在CO32-、SiO32-;X与硝酸钡溶液反应生成气体A、溶液B和沉淀C,则C一定是硫酸钡,一定含有SO42-,则一定不存在Ba2+。A一定是NO,在空气中转化为红棕色NO2,这说明含有还原性离子亚铁离子,因此一定不存在NO3-;溶液B与过量氢氧化钠反应生成气体D是氨气,一定存在铵根离子,沉淀E一定是氢氧化铁,与盐酸反应生成氯化铁,G是剩余盐酸和氯化铁的混合溶液。溶液F中通入过量的CO2生成沉淀H,H是氢氧化铝,所以原溶液中含有铝离子,其中铁离子不能确定。
(1)由题给信息可知,溶液X中确定不存在的阴离子有CO32-、SiO32-、NO3-。(2)根据以上分析可知沉淀C是BaSO4,由此可确定溶液X中肯定不存在的阳离子有Ba2+。(3)气体A是NO,产生气体A的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O。(4)由于溶液B中含有由Fe2+氧化得到的Fe3+,故无法确定溶液X中是否存在Fe3+;(5)根据以上分析可知步骤④中发生反应的离子方程式为AlO2-+CO2+2H2O=A l(OH)3↓+ HCO3-。(6)根据以上分析可知溶液X中肯定存在的离子有Al3+、NH4+、SO42-、Fe2+,可能存在的离子有Fe3+。检验铁离子是否存在的方法是:取少量溶液X于试管中,滴加几滴KSCN溶液,若溶液变红色,则溶液X中含有Fe3+;若溶液不变红色,则溶液X中不含有Fe3+。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)H2(g)+I2(g),2s时生成0.1mol H2 , 则以HI表示该时段的化学反应速率是( )
A.0.05 molLˉ1sˉ1
B.0.1 molLˉ1sˉ1
C.0.2 molLˉ1sˉ1
D.0.8 molLˉ1sˉ1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式或化学方程式,正确的是
A. 氯气通入水中:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 向 Fe(NO3)2 稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
C. 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++H2O
D. 向石灰水中加入过量NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的数值为NA。下列说法正确的是
A. 1 L 1 mol·L-1的NaHSO3溶液中含有的离子数为3NA
B. 2.24 L CO2与足量的Na2O2反应,转移电子数为0.1NA
C. 5.6 g乙烯和环丙烷的混合物中含C—H键数目为0.8NA
D. 常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCI)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从某酸性废液(主要含Cu2+、Fe3+、H+、Cl-中制备氯化亚铜。

请回答下列问题:
(1)出步驟①中发生的两个主要反应的离子方程式:________________________。
(2)步骤②的操作名称是___________。
(3)步骤④中所加物质X为___________。
(4)步骤⑤的操作是___________。
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是___________。
(6)在CuCl的生成过程中,可以循环利用的物质是______,理论上______ (填“是”或“否”)需要补充(不考虑调节等消耗):理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都是金属,把A浸入C的盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C金属的活动性顺序为 ( )
A. A>B>C B. A>C>B C. B>C>A D. B>A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定体积的密闭容器中,加入4molA和2molB发生反应:2A(g)+B(g)![]() 3C(g)+D(g),达到平衡时C的浓度为wmol/L。若维持体积和温度不变按下列四种方式加入起始量,达平衡后,C仍为wmol/L的是
3C(g)+D(g),达到平衡时C的浓度为wmol/L。若维持体积和温度不变按下列四种方式加入起始量,达平衡后,C仍为wmol/L的是
A. 8molA+4molB B. 4mol A+2mol B+6mol C+2mol D
C. 6molC+2molD+2molB D. 6mol C+2mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 常温下64 g S4和S8混合物中含有原子数为2NA
B. 标准状况下,22.4LHF中含电子数为10NA
C. l L1 mol/L的盐酸溶液中,所含氯化氢分子数为NA
D. 足量铁在1mol氯气中加热反应,铁失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( ) 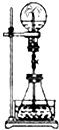
A.Cu与稀盐酸
B.NH4HCO3与稀盐酸
C.CaCO3与稀硫酸
D.NaHCO3与NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com