
【题目】(1)S2-、Fe2+、Fe3+、Mg2+、S、I-、H+,其中只有氧化性的是 ,只有
还原性的是 ,既有氧化性又有还原性的是 。
(2)氧化还原反应3S+6KOH=K2S+K2SO3+3H2O中,氧化产物是 ,该反应的
离子方程式为: 。
(3)已知 F是氧化性最强的元素,在与其他元素化合时只表现出负价,在3BrF3+5H2O=Br2+HBrO3+O2↑+9HF反应中,若有27克H2O参加反应,则被水还原的BrF3的分子数为 。
【答案】(1)Fe3+、Mg2+、H+;S2-、I-;Fe2+、S
(2)K2SO3;3S+6OH-=2S2-+SO32-+3H2O(3)0.4NA
【解析】
试题分析:元素处于最高价时只有氧化性,其中只有氧化性的是Fe3+、Mg2+、H+;元素处于最低价时只有还原性,只有还原性的是S2-、I-;元素处于中间价时既有氧化性又有还原性,既有氧化性又有还原性的是Fe2+、S;(2)氧化还原反应3S + 6KOH = K2S + K2SO3 + 3H2O中,元素化合价升高得到的产物是氧化产物,氧化产物是K2SO3,该反应的离子方程式为3S+6OH-=2S2-+SO32-+3H2O。(1)根据方程式3BrF3+5H2O=Br2+HBrO3+O2↑+9HF,当有5mol水参加反应时,O元素化合价由-2价升高到0价,2mol水被氧化,失去4mol电子,Br元素化合价由+3价降低到0价,则由H2O还原的BrF3为![]() mol,若有27克H2O参加反应,则被水还原的BrF3的物质的量为x,则
mol,若有27克H2O参加反应,则被水还原的BrF3的物质的量为x,则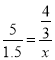 ,x=0.4mol,分子数为0.4NA。
,x=0.4mol,分子数为0.4NA。


科目:高中化学 来源: 题型:
【题目】对于反应2SO2(g)+O2(g)2SO3(g),能增大正反应速率的措施是( )
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶练铜的工艺流程如下:
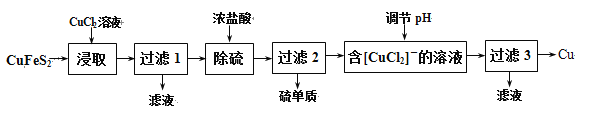
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有 ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为 。
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
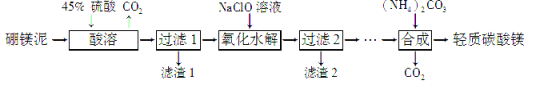
(1) 写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式 。
(2) 滤渣2的主要成分有MnO2和_____________,写出生成MnO2的离子方程式____________________。
(3)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________(只需写出相应的化学方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法是分析化学中常用实验方法,请根据滴定法的有关知识回答下列问题:
Ⅰ、某学生用0.1 mol·L-1 的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上1~2cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)_________AF。
(2)上述B步骤操作的目的是______________。
(3)在进行C步操作滴定前排气泡时,应选择下图2中的__________(填序号),若用25mL滴定管进行实验,当滴定管中的液面在“10”处,则管内液体的体积(填序号)__________(①=10mL,②=15mL,③<10mL,④>15mL)。

(4)判断以下操作,对测定结果盐酸浓度的影响(填“偏高”、“偏低”或““无影响”)
①上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是_________。
②若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是___________。
③如果滴定前装有待测溶液的酸式滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将____________。
Ⅱ、氧化还原滴定法实际生产中运用较为广泛的方法。制备纳米TiO2的方法之一是TiCl4在加热条件下水解生成TiO2·xH2O,经过过滤、水洗除去其中的Cl-,再经烘干、焙烧除去水分,最后得到粉体TiO2。
可用氧化还原滴定法测定TiO2的质量分数。在一定条件下,将粉体溶解并将溶液中的Ti2-氧化为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。【注:NH4Fe(SO4)2是一种复盐,含有两种阳离子】。请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为_______________________。
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量稀H2SO4的原因是____________________,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需用到图中的______________(填序号)
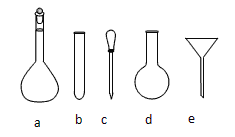
检验TiO2·xH2O中Cl-是否被除净的方法是________________________。
(3)滴定终点的现象是:当滴入最后一滴NH4Fe(SO4)2标准溶液时_______________________。
(4)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)粉体试样wg,消耗v ml c mol·L-1 NH4Fe(SO4)2标准溶液。则TiO2质量分数表达式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组在网上收集到信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入盛满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是: 。
(2)燃烧的本质是 。
(3)2010年8月初发生的俄罗斯森林大火的着火面积比伦敦市的面积还要大。控制森林火灾是世界性难题。根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延 _。
【提出假设】
假设1:白色物质是Na2O
假设2:白色物质是Na2CO3
假设3:白色物质是Na2O和Na2CO3的混合物
【设计实验方案·验证假设】该小组对燃烧后的白色产物进行如下探究:
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【思考与交流】
(4)甲同学认为由方案1得出结论不严密,请解释原因 。
(5)乙同学认为方案2得到的结论正确,白色物质为 。
(6)通过方案1和方案2的实验,你认为上述三个假设中, 成立。你的理由是 。
(7)钠在二氧化碳中燃烧的化学方程式为 。
(8)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 氢氧化钠可用食物调整碱性的添加剂
B. 棉、麻完全燃烧可以生成CO2和H2O
C. 脂肪在一定条件下都能发生水解反应
D. 汽油、柴油、煤油的主要成分都是碳氢化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_____________。

(2)按下图装置进行NH3性质实验。
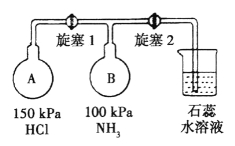
①先打开旋塞1,B瓶中的现象是_______________,原因是____________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_____________。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、PH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。

③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率为______________ (只列出算式,忽略水自身电离的影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于在密闭容器中、一定条件下进行的可逆反应N2(g)+3H2(g)![]() 2NH3(g),能说明反应已达到平衡状态的是
2NH3(g),能说明反应已达到平衡状态的是
A. 各物质体积分数相等 B. c(NH3)保持不变
C. 各物质浓度相等 D. c(NH3)∶c(N2)∶c(H2)=2∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(HF)2(g) ![]() 2HF(g) ΔH>0,且平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) ΔH>0,且平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
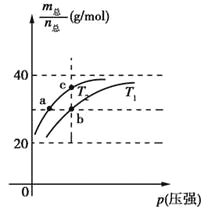
A.温度:T1<T2 B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:vb>va D.当![]() =30g·mol-1时,n(HF):n[(HF)2]=2:1
=30g·mol-1时,n(HF):n[(HF)2]=2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com