
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有
( )。
①0.2 mol H2O2完全分解转移的电子数为0.4NA
②25 ℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA
③将含0.1 mol FeCl3的 饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1 mol N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
A.①②③ B.①②④ C.①②③④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族.
(1)D在周期表中的位置 ;B的原子核外电子排布示意图 ;
(2)E元素形成最高价氧化物对应水化物对应的水化物的化学式为 ;
(3)元素C、D、E形成的原子半径大小关系是 (用元素符号表示)。
(4)C、D可形成化合物D2C2,D2C2含有的化学键是 ;
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式 ,
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
A.原混合溶液中c(K+)为0.2 mol·L-1 B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为 ,与电源负极相连的电极附近,溶液pH (选填“不变”“升高”或“下降”)。
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是 (选填a,b,c多选扣分)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 (选填a、b、c多选扣分)。
a.先加NaOH,后加Na2CO3,再加钡试剂 b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 ___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表的一部分。请回答:
| ① | |||||||||||||||||
| ③ | ④ | ⑤ | ⑥ | ||||||||||||||
| ② | ⑦ | ||||||||||||||||
| ⑧ | |||||||||||||||||
(1)元素③与⑧的元素符号分别为 、 。
(2)元素①②⑥形成的化合物的电子式 。
(3)元素①⑤⑥形成的共价化合物的化学式 。
(4)元素④⑤⑥⑦的第一电离能由大到小的顺序是 (写元素符号)。(5)元素①④形成的δ键与π键个数比为5:1的化合物是 (填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收。利用如图所示装置加热硫酸铜粉末直至完全分解。若硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如表所示。
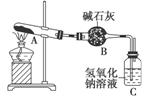
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.5 g | 140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是( )
A.4CuSO4
 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑
B.3CuSO4
 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑
C.5CuSO4
 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑
D.6CuSO4
 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各原子或离子的电子排布式错误的是 ( )
A. Na+: 1s22s22p6 B. F :1s22s22p5
C. O2—: 1s22s22p4 D. Ar: 1s22s22p63s23p6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com