
【题目】关于有机物a(![]() )、b(
)、b(![]() )、c(
)、c(![]() )的说法正确的是( )
)的说法正确的是( )
A.a、b、c的分子式均为C8H8
B.a、b、c均能与溴水发生反应
C.a、b、c中a,c能使高锰酸钾溶液褪色
D.a、b、c的一氯代物中,b有1种,a、c均有5种(不考虑立体异构)
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示。

下列有关化合物X的说法正确的是
A. 分子中两个苯环一定处于同一平面
B. 不能与饱和Na2CO3溶液反应
C. 1 mol化合物X最多能与2 molNaOH反应
D. 在酸性条件下水解,水解产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L带气压计的恒容密闭容器中通入2molX(g)和1molY(g),发生反应:2X(g)+Y(g)![]() 2Z(g);△H<0。若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。
2Z(g);△H<0。若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。
(1)若反应经历5min达到平衡,则Y的平均反应速率为___。
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图象如图甲。
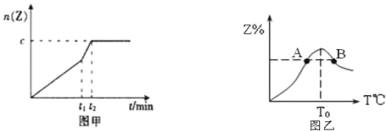
若c=0.90mol,t1时刻改变的条件是___(填选项编号,A.升温B.降温C.加压D.减压E.加催化剂),t2___5min(填“>”,“<”或“=”下同)。
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量___0.9mol(填“>”,“<”或“=”)。
(4)若将物质的量均为3.00mol物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。
①A、B两点Z物质正反应速率的大小关系是___;
②温度T<T0时,Z%逐渐增大的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究苯与溴的取代反应,有如下两个装置:

甲用装置Ⅰ进行如下实验,将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)①中的有机反应方程式为_________________________。
(2)①中长导管的作用是_______________________ 。
(3)烧瓶中生成的红褐色油状液滴的成分是____________________,要想得到纯净的产物,可用______________________试剂洗涤。
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。
可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳.
a的作用是___________________。b中的试剂是______________________。
(5)比较两套装置,装置Ⅱ的主要优点是___________________。(至少打出两点)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结晶玫瑰是一种具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)
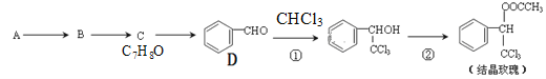
请回答下列问题:
(1)已知A是苯的一种同系物,写出A的结构简式____________。C7H8O
(2)C的同分异构体中,属于芳香族化合物的还有________种。
(3)检验D中含氧官能团的试剂名称为_______________,①的反应类型是____________。
(4)写出②的化学方程式____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种优良的消毒剂,其溶解度约是Cl2的5倍,但温度过高浓度过大时均易发生分解,因此常将其制成KClO2固体,以便运输和贮存。制备KClO2固体的实验装置如图所示,其中A装置制备ClO2,B装置制备KClO2。请回答下列问题:

(1)A中制备ClO2的化学方程式为__。
(2)与分液漏斗相比,本实验使用滴液漏斗,其优点是__。加入H2SO4需用冰盐水冷却,是为了防止液体飞溅和__。
(3)实验过程中通入空气的目的是__,空气流速过快,会降低KClO2产率,试解释其原因__。
(4)ClO2通入KOH溶液生成KClO2的同时还有可能生成的物质__。
a.KCl b.KClO c.KClO3 d.KClO4
(5)KClO2变质分解为KClO3和KCl,取等质量的变质前后的KClO2试样配成溶液,分别与足量的FeSO4溶液反应消耗Fe2+的物质的量__(填“相同”、“不相同”“无法确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
碱式碳酸镍的制备:
工业用电解镍新液(主要含NiSO4,NiCl2等)制备碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O],制备流程如图:
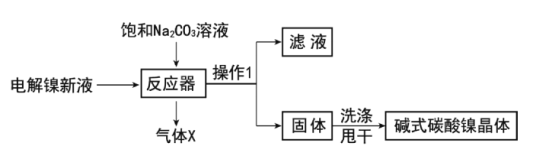
(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3·2Ni(OH)2+3Na2SO4+2X,X的化学式为__。
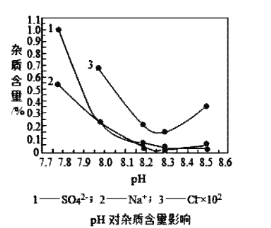
(2)物料在反应器中反应时需要控制反应温度和pH值。分析如图,反应器中最适合的pH值为__。
(3)检验碱式碳酸镍晶体洗涤干净的方法是__。
测定碱式碳酸镍晶体的组成:
为测定碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O]组成,某小组设计了如图实验方案及装置:
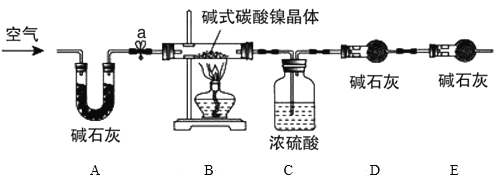
资料卡片:碱式碳酸镍晶体受热会完全分解生成NiO、CO2和H2O
实验步骤:
①检查装置气密性;
②准确称量3.77g碱式碳酸镍晶体[xNiCO3·yNi(OH)2·zH2O]放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量并记录;
④__;
⑤打开弹簧夹a缓缓鼓入一段时间空气;
⑥分别准确称量装置C、D、E的质量并记录;
⑦根据数据进行计算(相关数据如下表)
装置C/g | 装置D/g | 装置E/g | |
加热前 | 250.00 | 190.00 | 190.00 |
加热后 | 251.08 | 190.44 | 190.00 |
实验分析及数据处理:
(4)E装置的作用__。
(5)补充④的实验操作___。
(6)通过计算得到碱式碳酸镍晶体的组成__(填化学式)。
镍的制备:
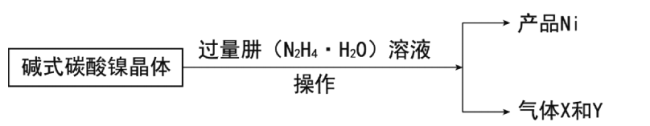
(7)写出制备Ni的化学方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知两个醛分子在NaOH溶液作用下可以发生加成反应,生成一种羟基醛,再加热脱水可生成烯醛类化合物:CH3CHO+CH3CHO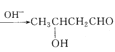
肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
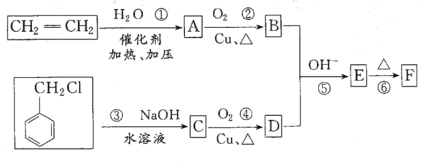
请回答:
(1)肉桂醛F的结构简式为____。E中含氧官能团的名称为____。
(2)写出下列转化的化学方程式
②_____。
③_____。
(3)符合下列要求的E物质的同分异构体有____种(苯环上有两个取代基,其中有一个甲基在对位且属于酯类)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液中粒子浓度的关系式中,正确的是( )

A.pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
D.图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com