
【题目】为探究外界条件对反应:mA(g)+nB(g)cZ(g) ΔH 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是 ( )
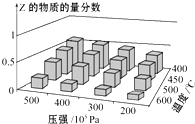
A.在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数不变
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.ΔH>0,m+n>c
D.温度不变,增大压强,平衡正向移动,达新平衡时,A的浓度比原平衡减小
【答案】A
【解析】
在恒温环境下,压强增大,Z的物质的量增大,平衡正向移动,根据勒夏特列原理可知,m+n>c;在恒压环境下,温度升高,Z的物质的量减小,平衡逆向移动,根据勒夏特列原理,反应放热,据此回答问题。
A.在恒温恒压条件下,向已达到平衡的体系中加入少量Z,为保持压强不变体积增大,由于生成物只有一种,故投料配比与原投料相同,达新平衡时与原平衡等效,Z的物质的量分数不变,A正确;
B.根据有效碰撞理论,升高温度,正、逆反应速率都增大,但是平衡逆向移动,平衡常数减小,B错误;
C.正反应是放热的,则△H<0,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c, C错误;
D.根据图像可知,若保持温度不变时增大压强,因体积减小,各组分的浓度变大,虽然平衡正向移动,但是根据平衡移动原理可知,达新平衡时,A的浓度比原平衡增大,D错误。
答案为A。


科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中M、W、T、L为同一短周期元素,L核外最外层电子数是W核外电子数的一半。下列叙述正确的是
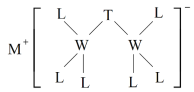
A.化合物ML属于离子化合物,也属于弱电解质
B.该新化合物中T满足8电子稳定结构
C.W的最高价氧化物可以与水反应生成弱酸
D.元素非金属性的顺序为W>T>L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的能量变化符合如图所示关系的是

A.CaCO3![]() CaO + CO2↑
CaO + CO2↑
B.2CH3CH2OH + O2![]() 2CH3CHO+ 2H2O
2CH3CHO+ 2H2O
C.2NH4Cl+ Ba(OH)2 = BaCl2+ 2NH3 H2O
D.2Na+2H2O =2NaOH + H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
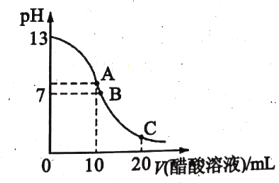
【题目】中和滴定是实验室定量测定未知酸或碱浓度的重要方法。25℃时,向 20.00 mL NaOH溶液中逐滴滴入某浓度的CH3COOH溶液以测定该醋酸溶液的浓度。滴定过程中,溶液的pH与滴入CH3COOH 溶液的体积关系如图所示, 回答下列问题:
(1)滴定时,使用到的主要玻璃仪器有__________。
(2)选择的指示剂是_________,如何判断滴定达到终点 _____________。
(3)若当滴定达到终点时,测得消耗 CH3COOH 溶液的体积为 10.00 mL. 则所测醋酸溶液的浓度为 _________molL-1。
(4)图中B 点所示溶液中c(Na +)______c(CH3COO-)(填“>”“<”或“=”)。
(5)图中 C 点对应的pH=4.7,该点所示溶液中c(CH3COO-)+ c(OH-)-c(Na+)=________ molL-1(已知:lg2=0.3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.H2(g)的燃烧热△H=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g) △H=+571.6 kJ/mol
B.反应物的总能量低于生成物的总能量时,该反应为放热反应
C.由石墨比金刚石稳定可知:c(金刚石,s)=c(石墨,s) △H<0
D.已知:298K时,N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物阿司匹林可由水杨酸制得,它们的结构如图所示有关说法正确的是
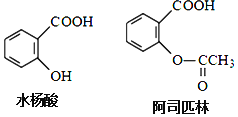
A.服用阿司匹林,身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液
B.阿司匹林的分子式为C9H10O4
C.水杨酸可以发生取代、加成、氧化、加聚反应
D.1mol阿司匹林最多可消耗2molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO![]() +2H2O
+2H2O
B.二氧化硫与酸性高锰酸钾溶液反应:5SO2+2H2O+2MnO![]() =2Mn2++5SO
=2Mn2++5SO![]() +4H+
+4H+
C.Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O![]() +6H+=2S↓+3H2O
+6H+=2S↓+3H2O
D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C, 在 0. 1 mol L-1 的CH3COOH 溶液中滴加 NaOH溶液,溶液中c(CH3COOH)、c(CH3COO-)与 pH的关系如图所示。下列叙述正确的是
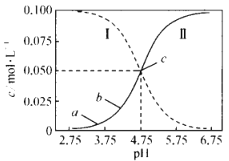
A.曲线I表示混合溶液中c(CH3COO-)随pH变化关系
B.a点溶液的导电能力比b点的强
C.25℃时,CH3COOH的电离平衡常数为10-4.75
D.pH=5.5的溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.0.1mol·L-1NaOH溶液:Na+、K+、![]() 、
、![]()
B.0.1mol·L-1Fe2(SO4)3溶液:Cu2+、![]() 、SCN-、
、SCN-、![]()
C.0.1mol·L-1Na2S溶液:Na+、K+、ClO-、OH-
D.0.1mol·L-1NH4HCO3溶液:Ba2+、K+、OH-、![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com