
ú�����г����о���ͬ�¶���ƽ�ⳣ����Ͷ�ϱȵ����⡣
��֪��CO (g) +H2O (g) H2 (g) +CO2 (g)ƽ�ⳣ��K���¶ȵı仯���±���
H2 (g) +CO2 (g)ƽ�ⳣ��K���¶ȵı仯���±���
�ش���������
��1���÷�Ӧ��ƽ�ⳣ������ʽK= ����H= 0(�<������>������=����
��2������һ���¶��£�C(s) +CO2 (g) 2CO (g)ƽ�ⳣ��K1��
2CO (g)ƽ�ⳣ��K1��
C (s) +H2O(g) CO(g) +H2 (g)ƽ�ⳣ��K2��K��K1��K2,֮��Ĺ�ϵ�� :
CO(g) +H2 (g)ƽ�ⳣ��K2��K��K1��K2,֮��Ĺ�ϵ�� :
��3��8000Cʱ����һ��10L�ĺ��ݷ�Ӧ���г���0.40molCO��1.60molˮ��������һ��ʱ���Ӧ�ﵽƽ�⣬��ʱCO��ת����Ϊ �������������������䣬��ƽ����ϵ����ͨ��0. 10molCO��0.40molCO2����ʱv�� v�� (�>������=����<������
(7��)��1�� C��CO2��C��H2��/C��CO�� C��H2O��,(1��) ��< (1��)��
��2�� K��K2/K1 (1��) ��3��80% (2��)����(2��)
���������������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�Ļ�ѧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ������ʽK�� �����ݱ��е����ݿ�֪�������¶ȵ����ߣ�ƽ�ⳣ��K�Ǽ�С�ģ���˵�������¶�ƽ�����淴Ӧ������У���������Ӧ�Ƿ��ȷ�Ӧ������H��0��
�����ݱ��е����ݿ�֪�������¶ȵ����ߣ�ƽ�ⳣ��K�Ǽ�С�ģ���˵�������¶�ƽ�����淴Ӧ������У���������Ӧ�Ƿ��ȷ�Ӧ������H��0��
��2�����ݸ�˹���ɿ�֪���ڣ��ټ��õ���ӦCO (g) +H2O (g) H2 (g) +CO2 (g)������ƽ�ⳣ��֮��Ĺ�ϵ��K��K2/K1��
H2 (g) +CO2 (g)������ƽ�ⳣ��֮��Ĺ�ϵ��K��K2/K1��
CO (g) +H2O (g) H2 (g) +CO2 (g)
H2 (g) +CO2 (g)
��ʼŨ�ȣ�mol/L�� 0.040 0.16 0 0
ת��Ũ�ȣ�mol/L�� x x x x
ƽ��Ũ�ȣ�mol/L�� 0.040��x 0.16��x x x
����ݸ��¶��µ�ƽ�ⳣ����֪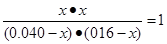
���x��0.032mol/L
����CO��ת���ʣ�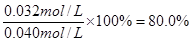
�����������������䣬��ƽ����ϵ����ͨ��0. 10molCO��0.40molCO2�����ʱCO��H2O��CO2��H2��Ũ�ȷֱ��ǣ�mol/L��0.018��0.128��0.072��0.032������Q�� �����Է�Ӧ��Ȼ��ƽ��״̬�������淴Ӧ������ȡ�
�����Է�Ӧ��Ȼ��ƽ��״̬�������淴Ӧ������ȡ�
���㣺������淴Ӧƽ�ⳣ���ļ��㡢�жϺ�Ӧ��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������͡����������ǿ����Ҫ�ǿ���ѧ����ƽ�ⳣ�����塢����ʽ�Լ��й�Ӧ�õ���Ϥ�˽�̶ȣ�ּ������ѧ������˼ά�����淶�����������ڽ��п��淴Ӧ���йؼ���ʱ��һ����á�����ʽ�����У����ֱ��г���ʼ����ת������ƽ������ij��̵�����Ȼ��������֪������ʽ���㼴�ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ѧ����Դ����������������ʮ�ֹؼ������á�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϡ�
I������ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ�����ͼʵ�飨ͼ�����õ缫��Ϊ���Ե缫����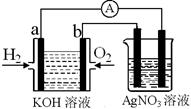
��1����������ȼ�ϵ���У����б��ﲻ��ȷ����________
| A��a�缫�Ǹ�����OH���������� |
| B��b�缫�ĵ缫��ӦΪ��O2��2H2O��4e����4OH�� |
C������ܷ�ӦʽΪ��2H2+O2 2H2O 2H2O |
| D���������Һ��pH���ֲ��� |
 2NH3(g) ��H����92.20 kJ��mol��1��
2NH3(g) ��H����92.20 kJ��mol��1��| ʱ�䣨h�� ���ʵ�����mol�� | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ˮú��ת����ӦCO(g)+H2O(g)  CO2(g)+H2 (g)��һ���¶��´ﵽ��ѧƽ��״̬��
CO2(g)+H2 (g)��һ���¶��´ﵽ��ѧƽ��״̬��
���������գ�
��1��д���÷�Ӧ��ƽ�ⳣ������ʽK=________________��
��2��һ���¶��£���һ���ݻ�������ܱ������з���������Ӧ������˵�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� ��ѡ���ţ���
a�������е�ѹǿ���� b��1 mol H��H�����ѵ�ͬʱ����2 molH��O��
c��v��(CO) = v��(H2O) d��c(CO) = c(H2)
��3������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ�����ʵ����1��ʵ����2�����ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 3 |
| 2 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 3 | 950 | 1 | 2 | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ�������£�NO��NO2��Ͽ�����N2O3����Ӧ�Ļ�ѧ����ʽΪ��NO(g)+NO2(g) N2O3(g) ��H<0
N2O3(g) ��H<0
��ͼ��ʾһ������NO��NO2������巢����Ӧʱ��NO2Ũ����ǰ25s�ڵı仯���÷�Ӧ���е�45sʱ�ﵽƽ�⣬���NO2Ũ��ԼΪ0.010mol/L��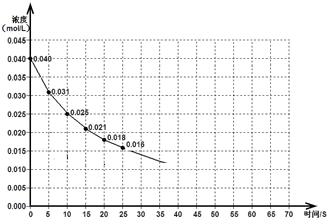
��1��ǰ20s�ڣ�NO2��ƽ����Ӧ����Ϊ_________________��
��2�������������䣬�������¶ȣ�NO2��ת����_______ �����������С�����䡱����
��ѹ������������÷�Ӧƽ����_______�ƶ��������������
��3������Ӧ������70�룬���ڴ��ͼ�л���25����70��ķ�Ӧ�������ߡ�
��4�����ڷ�Ӧ��ʼʱ�������(��������������)�����ڴ��ͼ�л����Ӵ�����ķ�Ӧ�������ߡ�
��5��NO��NO2�Ļ��������NaOH��Һ���գ��õ�����ֻ��һ�֣���÷�Ӧ�����ӷ���ʽΪ��___________________________________���÷�Ӧ����������______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ش��������⣺
��1���ֱ���Ũ��ϡ�����ܽ����������ͭ�ۣ�������������ʵ������ٵ���____ ���ᣨ�Ũ����ϡ��������Ӧ�����ӷ���ʽ�� ��
��2�� 800��ʱ����2 L�ĺ����ܱ������г���2 mol NO��1mol O2������Ӧ��2NO��g��+O2��g�� 2NO2��g������5min�ﵽƽ�⣬���c��NO��=0��5mol/L��������Q kJ��
2NO2��g������5min�ﵽƽ�⣬���c��NO��=0��5mol/L��������Q kJ��
��5 min�� v��O2��= ��
�ڸ������£�2NO��g��+O2��g�� 2NO2��g���ġ�H= ��
2NO2��g���ġ�H= ��
������ƽ���������ٳ���NO��NO21mol����ʱv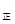 v
v ���>������=����<������
���>������=����<������
������ƽ�������н�����1mol NO2��ƽ����____ ������������������ƶ�������ƽ��ʱ��NO2���������____ �����������С�����䡱����
��3��Ⱦ�Ϲ�ҵ�ŷŵķ�ˮ�к��д����ж���NO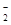 ��������ǿ���������¼������۳�ȥ����Ӧ����������̬�������ɡ����ȷ�Ӧ�����Һ����ʹʪ��ĺ�ɫʯ����ֽ�����������ݳ�������д���÷�Ӧ�����ӷ���ʽ____ ��
��������ǿ���������¼������۳�ȥ����Ӧ����������̬�������ɡ����ȷ�Ӧ�����Һ����ʹʪ��ĺ�ɫʯ����ֽ�����������ݳ�������д���÷�Ӧ�����ӷ���ʽ____ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ���¶�ʱ�����ݻ�һ�����ܱ������У���ӦA(��)��B(g)  C(g)��D(g)�ﵽƽ��������¶�������������ܶ�������ش��������⣺
C(g)��D(g)�ﵽƽ��������¶�������������ܶ�������ش��������⣺
��1������Ӧ�� ������ȡ������ȡ�����Ӧ���÷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽ�� ��
��2�����жϸ÷�Ӧһ���ﵽƽ��״̬�������� ������д��ĸ��ţ�
A������������C����D��
B����λʱ��������n molA��ͬʱ����n molC
C���¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯
D���¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯
��3���÷�Ӧ������Ӧ������ʱ��仯�Ĺ�ϵ��ͼ��ʾ��t2ʱ����ij���������ı�������� ������д��ĸ��ţ�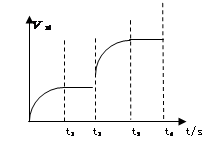
A������ B����ѹ C������ D������A����
��4�������¶ȵ�T��ʱ����һ�ܱ������г���2mol A��3mol B������������Ӧ��ƽ�����K=1��Ȼ�����¶Ȳ��������£����������ݻ���ԭ����10�������A�İٷֺ���ʼ��δ�ı䣬���ʱB��ת������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ������SO2�ͺ�0.7mol�����Ŀ���(����CO2)����0.5 L�ܱ������ڣ�550��ʱ���ڴ��������·�����Ӧ��2SO2(g)��O2(g) 2SO3(g)(����Ӧ����)�����n(O2)��ʱ��ı仯���±�
2SO3(g)(����Ӧ����)�����n(O2)��ʱ��ı仯���±�
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
(18��)�����Ԫ�صĵ��ʼ��仯���ﱻ�㷺Ӧ���������������С�
��һ������Na������O2�г��ȼ�գ��μӷ�Ӧ��O2���Ϊ5.6 L(��״��)����÷�Ӧ������ת�Ƶ��ӵ���ĿΪ_________��
��2������﮹㷺Ӧ���ڻ�ѧ��Դ���죬�ˮ��ؾ������е�һ�ֲ�Ʒ���õ���Խ���﮺� �ְ�Ϊ�缫���ϣ���LiOHΪ����ʣ�����ˮ���ɷŵ硣
�ܷ�ӦΪ��2Li+2H2O=2LiOH+H2��
���ˮ��طŵ�ʱ��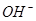 ��_________���ƶ���
��_________���ƶ���
��д���õ�طŵ�ʱ�����ĵ缫��Ӧʽ��_________________��
�۵������LiCl�����Ʊ�����Li����LiC1�۵���873 K���ϣ������µ�⣬����Li�������͡�������ѧ�Ҳ����о������ֵ��LiCl��KCl�����λ��������ڽϵ��¶������ɽ���Li��
��������������KCl��������_________________________________________��
д���������λ��������������ĵ缫��Ӧʽ��______________________________��
��3�������о������������ؿ�����ҵ����Ȼ�����������Ĵ������йط�ӦΪ�� ��һ���¶��£���2 L�ݻ�������ܱ������г���4 mol
��һ���¶��£���2 L�ݻ�������ܱ������г���4 mol 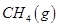 ��6 mo1 H2O(g)������Ӧ��10 minʱ����Ӧ�ﵽƽ��״̬�����CH4(g)��H2(g)�����ʵ�����ʱ��仯��������ͼ��ʾ��
��6 mo1 H2O(g)������Ӧ��10 minʱ����Ӧ�ﵽƽ��״̬�����CH4(g)��H2(g)�����ʵ�����ʱ��仯��������ͼ��ʾ��
��0��10 min���� (CO)��ʾ�Ļ�ѧ��Ӧ����Ϊ_________��
(CO)��ʾ�Ļ�ѧ��Ӧ����Ϊ_________��
�����������У��ܹ�֤���÷�Ӧ�Ѵﵽƽ��״̬����_________(�����)��
a������3 molH-H����ͬʱ��4 molC-H������
b��������������ʱ����Ӧ��ϵ��ѹǿ���ֲ���
c����Ӧ���������������ֲ���
d��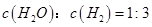
�۴��¶��£��÷�Ӧ�Ļ�ѧƽ�ⳣ��K=_________mo12��L-2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
����ʱ��N2O5�ɰ����зֽ⣺N2O5 N2O3 + O2��N2O3�ֿɰ����зֽ⣺ N2O3
N2O3 + O2��N2O3�ֿɰ����зֽ⣺ N2O3 N2O + O2���� 4 molN2O5����һ���ܱ������У������� t��ʱ��Ӧ�ﵽ��ƽ��״̬��ƽ��ʱ��c��O2��=" 4.5" mol/L, c��N2O3��=" 1.62" mol/L,c��N2O��= mol/L����ʱN2O5�ķֽ���Ϊ ��
N2O + O2���� 4 molN2O5����һ���ܱ������У������� t��ʱ��Ӧ�ﵽ��ƽ��״̬��ƽ��ʱ��c��O2��=" 4.5" mol/L, c��N2O3��=" 1.62" mol/L,c��N2O��= mol/L����ʱN2O5�ķֽ���Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com