
【题目】碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和_________。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代数关系式为_________________。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
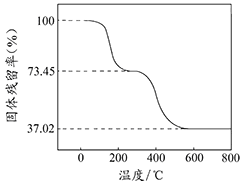
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO20.560L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在2700C时已完全失去结晶水,6000C以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-): n(CO32-)(写出计算过程)________。
【答案】阻止燃烧 2a+3b=c+2d 3:5(过程见解析)
【解析】
(1)碱式碳酸铝镁[MgaAlb(OH)c(CO3)dxH2O]受热分解最终生成MgO、Al2O3,MgO、Al2O3的熔点较高且都不燃烧,所以有阻燃作用,故答案为生成的产物具有阻燃作用;
(2)化合物中各元素化合价的代数和为0,所以2a+3b+c+4d=(c+3d)×2,所以得2a+3b=c+2d,故答案为2a+3b=c+2d;
(3)n(CO2)= ![]() =2.50×10-2mol,m(CO2)=2.50×10-2mol×44g/mol=1.10g,在270℃~600℃之间,失去结晶水后的样品进一步受热分解生成CO2、H2O,m(CO2)+m(H2O)=3.390g×(0.7345-0.3702)=1.235g,m(H2O)=1.235g-1.10g=0.135g,n(H2O)=
=2.50×10-2mol,m(CO2)=2.50×10-2mol×44g/mol=1.10g,在270℃~600℃之间,失去结晶水后的样品进一步受热分解生成CO2、H2O,m(CO2)+m(H2O)=3.390g×(0.7345-0.3702)=1.235g,m(H2O)=1.235g-1.10g=0.135g,n(H2O)=![]() =7.50×10-3 mol,再根据氢原子守恒得n(OH-)=2n(H2O)=1.50×10-2 mol,根据C原子守恒得n(CO32-)=n(CO2)=2.50×10-2mol,所以n(OH-):n(CO32-)=1.50×10-2 mol:2.50×10-2mol=3:5,答:碱式碳酸铝镁样品中的n(OH-):n(CO32-)=3:5。
=7.50×10-3 mol,再根据氢原子守恒得n(OH-)=2n(H2O)=1.50×10-2 mol,根据C原子守恒得n(CO32-)=n(CO2)=2.50×10-2mol,所以n(OH-):n(CO32-)=1.50×10-2 mol:2.50×10-2mol=3:5,答:碱式碳酸铝镁样品中的n(OH-):n(CO32-)=3:5。


科目:高中化学 来源: 题型:
【题目】痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小心涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线。用下列化学式表示这三种物质都正确的是 ( )
A.①AgNO3;②NaBr;③AgBr B.①AgNO3;②NaCl;③AgCl
C.①AgCl; ②AgNO3;③NaCl D.①AgNO3;②NaCl;③Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校课外活动小组仅有一大一小两试管和氢氧化钠溶液。甲、乙两个同学找来铝制废牙膏皮,各自设计了一套装置如下图,制取并收集一试管氢气。
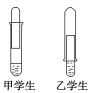
(1)哪个学生设计的装置比较合理?____(填“甲”或“乙”),另一设计装置不合理的原因____________
(2)用比较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是____。
(3)还可以用哪些常见物品和试剂代替废牙膏皮和氢氧化钠溶液完成实验?_____________
(4)测定H2和空气混合气体的爆炸范围实验如下所述。取10支大试管,依次盛水90%(体积分数)、80%……再用排水集气法收集H2,而后分别把试管口移近酒精灯火焰,实验结果如下:
H2体积分数/% | 90 | 80 | 70 | 60~20 | 10 | 5 |
空气体积分数/% | 10 | 20 | 30 | 40~80 | 90 | 95 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱爆炸 | 强爆炸 | 弱爆炸 | 不燃烧 不爆炸 |
由上述实验结果评价:用向下排空气法收集H2,保持试管倒置移近火焰,如果只发出轻微的“噗声”,表示收集的H2已纯净的说法的真正涵义:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某![]() 、
、![]() 的混合溶液中逐滴加入
的混合溶液中逐滴加入![]() 的盐酸,测得溶液中的
的盐酸,测得溶液中的![]() 、
、![]() 、
、![]() 、
、![]() 的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是
的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是![]()
![]() 已知:
已知:![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() ;
;![]() 的酸式电离平衡常数
的酸式电离平衡常数![]()
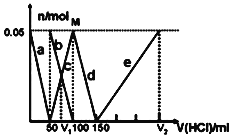
A.a曲线表示的离子方程式为:![]()
B.M点时生成的![]() 为
为![]()
C.原混合溶液中的![]() 与
与![]() 的物质的量之比为1:2
的物质的量之比为1:2
D.![]() :
:![]() :4
:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CCl3CHO可通过“CH3CH2OH+4Cl2→CCl3CHO+5HCl”进行制备。
⑴实验室常用KMnO4、MnO2或NaClO与浓盐酸反应制取Cl2。质量分数为36.5%,密度为1.18 g·cm-3盐酸,其物质的量浓度为______mol·L1。等物质的量的KMnO4、MnO2或NaClO与足量浓盐酸反应,理论上生成的Cl2的质量之比为______。
⑵可用如下方法测定所制CCl3CHO粗品的纯度(杂质不参与反应):称取该实验制备的产品5.00 g,配成100.00 mL溶液,取其中10.00 mL,加入一定量的NaOH后,加入30.00 mL 0.100 mol·L1的碘标准液,用0.100 mol·L1的Na2S2O3溶液滴定,重复上述3次操作,消耗Na2S2O3溶液平均体积为20.00 mL。实验中所发生反应如下:CCl3CHO+NaOH=CHCl3+HCOONa,HCOONa+I2=HI+NaI+CO2↑, I2+2Na2S2O3=2NaI+Na2S4O6,计算粗品中所含CCl3CHO的质量分数(写出计算过程)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是合成一种天然茋类化合物的重要中间体,其合成路线如下:
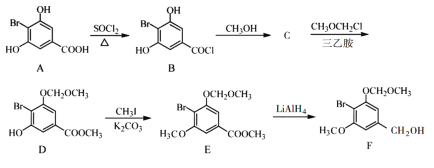
(1)A中含氧官能团的名称为_________。
(2)A→B的反应类型为________。
(3)写出B→C的化学反应方程式:________
(4)C→D的反应中有副产物X(分子式为C12H15O6Br)生成,写出X的结构简式:________。
(5)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________。
①能与FeCl3溶液发生显色反应;
②碱性水解后酸化,含苯环的产物分子中不同化学环境的氢原子数目比为1∶1。
(6)已知: (R表示烃基,R'和R"表示烃基或氢)
(R表示烃基,R'和R"表示烃基或氢)
写出以![]() 和CH3CH2CH2OH为原料制备
和CH3CH2CH2OH为原料制备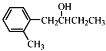 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)__________。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式为![]() ,下列对它的描述正确的是( )
,下列对它的描述正确的是( )
A. 它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B. 所有原子可能共平面
C. 易溶于水,也易溶于有机溶剂
D. 能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向KI溶液中滴入少量新制氯水和四氯化碳,振荡、静置,溶液下层呈紫红色 | I的还原性强于Cl |
B | 向无水乙醇中加入浓H2SO4,加热,将产生的气体通入酸性KMnO4溶液,紫红色褪去 | 该气体一定是乙烯 |
C | 测定Na2CO3和Na2SiO3溶液的pH,后者pH比前者的大 | C的非金属性比Si强 |
D | 向1-溴丙烷中加入KOH溶液,加热几分钟,冷却后再加入AgNO3溶液,无淡黄色沉淀生成 | 1-溴丙烷没有水解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,下列有关该物质的说法正确的是( )![]()

A.该物质的分子式为C16H18O3
B.该物质分子中的所有原子可能共平面
C.滴入KMnO4溶液,可观察到紫色褪去,证明结构中存在碳碳双键
D.1 mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4 mol、7 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com