
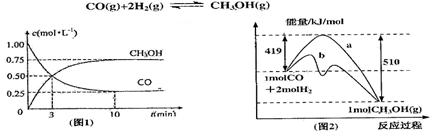
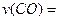 ��
��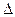 H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ�
H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ� ��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������
��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������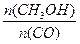 ����� ��
����� �� 
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cZ��g���ﵽƽ��ʱ��ƽ�ⳣ��ΪK1�����¶Ȳ���������½��������ѹ����ԭ����һ�룬�ﵽ�µ�ƽ���Y��Ũ��Ϊԭ����1��6����ƽ�ⳣ��ΪK2����K1 ��K2�Ĵ�С��ϵ�� �� ��
cZ��g���ﵽƽ��ʱ��ƽ�ⳣ��ΪK1�����¶Ȳ���������½��������ѹ����ԭ����һ�룬�ﵽ�µ�ƽ���Y��Ũ��Ϊԭ����1��6����ƽ�ⳣ��ΪK2����K1 ��K2�Ĵ�С��ϵ�� �� ��| A��K1��K2 | B��K1��K2 | C��K1��K2 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OH(g)���״���������ʱ��Ĺ�ϵ����ͼ��ʾ��
CH3OH(g)���״���������ʱ��Ĺ�ϵ����ͼ��ʾ��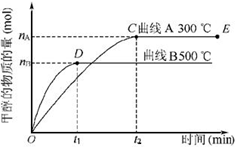
| A����300 �������£�t1ʱ�̸÷�Ӧ�ﵽ��ѧƽ�� |
| B����500 �������£��ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)ΪnB/(3t1) mol/L |
| C���������������������£�������E�����ϵ���ѹ����ԭ����1/2����������Ũ�ȼ�С |
| D����ͼ��˵���÷�Ӧ������ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH��g��
CH3OH��g��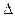 H1
H1 CH3OH��g��+H2O��g��
CH3OH��g��+H2O��g��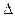 H2
H2| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
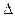 H1 ��(�>����=����<��)��
H1 ��(�>����=����<��)�� ��ijʱ�̲�ø���ֵ�Ũ�����£�
��ijʱ�̲�ø���ֵ�Ũ�����£�| ���� | H2 | CO | CH3OH |
| Ũ��/��mol��L��1�� | 0.2 | 0.1 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����
2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����| A����X�ķ�Ӧ����Ϊ0.2 mol��L��1��s��1����Z�ķ�Ӧ����Ϊ0.3 mol��L��1��s��1 |
| B�����������г��뺤����ѹǿ����Y��ת������� |
| C�������¶ȣ�����Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ� |
| D����ʼ���������е�X��Y���ʵ���֮��Ϊ2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
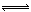 eC(g)+fD(g),����Ӧ������������������ʱ��C������������C%�����¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ.����������ȷ����
eC(g)+fD(g),����Ӧ������������������ʱ��C������������C%�����¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ.����������ȷ����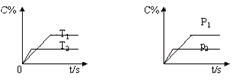
| A���ﵽƽ���,�������¶�,��ѧƽ�����淽���ƶ� |
| B����ƽ���,��ʹ�ô���,C���������������� |
| C����ѧ����ʽ��m+n>e+f |
| D���ﵽƽ���,����A���������ڻ�ѧƽ�����������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ɫ����ˮ���պ���ɫ��dz |
| B��������������Һ�У����������Է�ֹ�������� |
| C����������Ĺ�����ʹ�ù�����������߰����������� |
| D��ʵ���ҳ����ű���ʳ��ˮ�ķ����ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2C(g) ��2D(g)��2 min ĩ��Ӧ�ﵽƽ��״̬������0.8 mol D������д����հף�
2C(g) ��2D(g)��2 min ĩ��Ӧ�ﵽƽ��״̬������0.8 mol D������д����հף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g) ��H���D190 kJ��mol��1
2SO3(g) ��H���D190 kJ��mol��1 ����_______________��������ĸ��
����_______________��������ĸ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com