
| A、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
| B、SO2具有漂白性可以是酸性高锰酸钾溶液褪色 |
| C、实验室可用NaOH溶液处理NO2和SO2废气 |
| D、稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 |


科目:高中化学 来源: 题型:
| A、c (H+)×c(OH-)=10-14的溶液 |
| B、n(H+)=n(OH-) 的溶液 |
| C、c (H+)=1.0×10-7 mol/L的溶液 |
| D、pH=3的酸与pH=11的碱等体积混合后的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
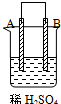 | 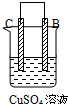 |  | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A、装置甲中的B金属是原电池的负极 |
| B、装置乙中的C金属是原电池的阳极 |
| C、装置丙中的D金属是原电池的正极 |
| D、四种金属的活泼性顺序是D>A>B>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | X | Y | Z | W |  |
| ① | CuO | Cu(OH)2 | CuSO4 | Cu | |
| ② | NaCl | NaHCO3 | Na2CO3 | NaOH | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | SO2 | H2SO3 | Na2SO3 | NaHSO3 |
| A、①②③ | B、①③④ |
| C、②③④ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,向l00mL 0.01mol?L-1HA溶液中逐滴加入0.02mol??L-1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是( )
常温下,向l00mL 0.01mol?L-1HA溶液中逐滴加入0.02mol??L-1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是( )| A、HA为一元强酸,MOH为一元强碱 |
| B、K点所示溶液中c(A-)>c(M+) |
| C、N点水的电离程度小于K点水的电离程度 |
| D、K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol??L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、给盛有液体的烧瓶加热时,需要加碎瓷片或沸石 |
| B、CCl4萃取碘水中碘的实验,分液时,水层应从分液漏斗下口放出,CCl4层从应上口倒出 |
| C、用容量瓶配制溶液,定容时加水超过了刻度线,必须进行重新配制 |
| D、测定溶液pH时,应用干燥洁净的玻璃棒蘸取溶液点在pH试纸上跟标准比色卡对照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用SO2漂白银耳 |
| B、用硫酸清洗锅炉中的水垢 |
| C、高温下用镁还原SiO2制取粗硅 |
| D、用Na2S作沉淀剂,除去废水中Cu2+和Hg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com