
(15分)三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到。
已知:白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3(三氯氧磷);POCl3能溶于PCl3;POCl3和PCl3遇水会强烈水解。实验室制取PCl3的装置示意图和有关数据如下:

物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
白磷 | 44.1 | 280.5 | 1.82 |
PCl3 | -112 | 75.5 | 1.574 |
POCl3 | 2 | 105.3 | 1.675 |
请回答:
(1)实验所需氯气可用MnO2和浓HCl反应制取,实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有 。制取的氯气需要进行干燥,请设计实验证明通入的氯气是干燥
的 (写出操作、现象、结论)。
(2)实验过程中要加入白磷、通入CO2、通入Cl2、加热,实验时具体的操作方法和顺序是 。
(3)E烧杯中加入冷水的目的是 ,干燥管中碱石灰的作用是 。
(4)实验制得的粗产品中常含有POCl3、PCl5等,先加入过量白磷加热,除去PCl5和过量白磷后,再除去PCl3中的POCl3制备纯净的PCl3可选用的方法有 (填字母序号)。
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,则PCl3和水反应后所得溶液中除OH-之外其它离子的浓度由大到小的顺序是 (已知亚磷酸(H3PO3)是二元弱酸)。
②若将0.01 mol POCl3投入热水配成1 L的溶液,再逐滴加入AgNO3溶液,则先产生的沉淀是 [已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10]。
(1)圆底烧瓶和分液漏斗 将气体通过装有无水硫酸铜的U形管(干燥管),若白色粉末未变蓝,则气体干燥 (或者通入装有干燥的有色布条的集气瓶,布条不褪色等,合理答案均可)
(2)先打开K2,等反应体系中充满CO2后,加入白磷,然后再打开K1,通入氯气,加热
(3)冷却收集PCl3 吸收多余的氯气和空气中的水蒸气
(4)C
(5)①c(H+)﹥c(Cl-)﹥c(H2PO3-)﹥c(HPO32-) ②AgCl
【解析】
试题分析:(1)实验室制取氯气用浓盐酸与MnO2 在加热的条件下进行,装置采用固体和液体加热制取气体的装置,所以实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有圆底烧瓶和分液漏斗,干燥的氯气没有漂白性,所以证明通入的氯气是干燥的方法是将氯气通入装有干燥的有色布条的集气瓶,布条不褪色,说明氯气是干燥的。
(2)PCl3遇O2会生成POCl3(三氯氧磷),所以向通入CO2 将空气赶走,白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5,然后在加入白磷,氯气最后通,白磷熔沸点低,最后加热,实验时具体的操作方法和顺序是先打开K2,等反应体系中充满CO2后,加入白磷,然后再打开K1,通入氯气,加热。
(3)PCl3 的沸点较低,所以E烧杯中加入冷水的目的是冷却收集PCl3,POCl3和PCl3遇水会强烈水解,干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气。
(4)根据表格提供的信息,它们互溶且熔沸点不同,所以除去PCl3中的POCl3制备纯净的PCl3可选用的方法是蒸馏法。
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,亚磷酸(H3PO3)是二元弱酸,分别电离,一步比一步艰难,而HCl是强酸,全部电离,所以离子的浓度由大到小的顺序是c(H+)﹥c(Cl-)﹥c(H2PO3-)﹥c(HPO32-),
②若将0.01 mol POCl3投入热水配成1 L的溶液,发生的化学反应为POCl3+H2O = H3PO4+3HCl,盐酸是强酸,Cl-浓度为0.03mol/L,H3PO4 是中强酸,分步电离,以第一步电离为主,产生的PO43-的浓度很小,根据Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10,逐滴加入AgNO3溶液,则先产生的沉淀是AgCl。
考点:考查氯气的实验室制法,PCl3的制备及性质检验,离子浓度的大小比较,沉淀溶解平衡等知识。


科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:填空题
(12分)(1)在配合物[Zn(NH3)4]2+中,提供空轨道的微粒是___________,在配合物物质[Co(NH3)5Cl]Cl2 中,配位数数值是_________(填数字)。
(2)根据价电子对互斥理论预测HCN的空间结构为 形,其中C原子用于形成σ键的是2个sp杂化轨道。(提示:HCN分子中所有原子的最外电子都达稳定结构。)
(3)在NaCl晶体中任一个Na+与它最近且等距离的Cl-有______个。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市高三一模理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.2014年德美科学家因开发超分辨率荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代。利用此类光学显微镜可以观察活细胞内蛋白质等大分子。
B.利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法
C.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料
D.分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三下学期第一次月考理科综合化学试卷(解析版) 题型:实验题
(14分)溴化钙是一种溴化物,用于石油钻井,也用于制造溴化铵及光敏纸、灭火剂、制冷剂等。制备CaBr2·2H2O的主要流程如下:

(1)与液溴的反应温度不能超过40℃的原因是 。
(2)滤渣的成分可能是 。
(3)试剂M是 ,加入M的目的是 。
(4)操作Ⅱ的步骤为蒸发浓缩、 、洗涤、干燥
(5)将氨气通入石灰乳,加入溴,于65°C进行反应也可制得溴化钙,此反应中还会生成一种无色气体,写出反应的化学方程式 。
(6)制得的CaBr2·2H2O可以通过以下方法测定纯度:称取5.00g样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却,称量。得到2.00g固体,则CaBr2·2H2O的质量分数为 。(相对原子质量:Ca—40 Br—80 H—1 O—16)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列判断正确的是
A.常温常压下,16g甲烷分子所含质子数为10NA
B.1 mol Cl2参加反应转移电子数一定为2NA
C.标准状况下,22.4L乙醇的分子数为NA
D.1 L 0.01 mol的Na2CO3溶液中含有0.01NA 个CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.稀硝酸中加入过量铁粉:Fe + 4H+ + NO=== Fe3+ + NO↑ + 2H2O
B.用铜作电极电解饱和食盐水:2Cl- + 2H2O 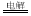 Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-
C.氯化铝溶液中加入过量氨水:Al3+ + 3NH3·H2O=== Al(OH)3 ↓+ 3NH
D.向BaCO3固体中加入过量的稀H2SO4:BaCO3+2H+===Ba2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省厦门市高三质量检查理综化学试卷(解析版) 题型:实验题
(15分)过硫酸钠( Na2S2O8)是一种重要化工原料。某研究小组进行如下实验
实验一 过硫酸钠的制取
采用下图装置制取Na2S2O8。

装置I中:主反应:(NH4)2S2O8 +2NaOH Na2S2O8+2NH3↑+2H2o
Na2S2O8+2NH3↑+2H2o
副反应:①2NH3+3Na2S2O8十 6NaOH===6Na2SO4 +6H2o十N2
6NaOH===6Na2SO4 +6H2o十N2
②3Na2S2O8 +3H2O+3Na2SO4+3H2SO4 +O3 ↑
(1)装置Ⅱ的作用是 。
(2)装置I还需补充的实验仪器或装置有_ (填序号)。
a.温度计 b.酒精灯 c.水浴 d.洗气瓶
(3)装置I发生反应的同时需要持续通入氮气的目的是
实验二过硫酸钠的性质实验
(4)为研究Na2S2O8溶解度随温度变化情况,实验过程需要测定的数据是 。
(5)Na2S2O8溶液与铜反应时先慢后快,除反应放热这一因素外,有人认为还有一种可能是反应生成的Cu2+对后续反应起催化作用,能检验该说法是否正确的实验方案为 。
实验三过硫酸钠的应用研究
(6)为检验用Na2S2O8溶液吸收NO的可行性,某同学设计下图所示实验(已知NO不溶于NaOH溶液)。实验步骤如下:
i.检查装置气密性,并按下图加人试剂;

ii.打开a和d,通人足量N2,关闭d;
iii.往装置中通人适量NO,关闭a;
iv.....
①步骤iv中,对分液漏斗的操作是 _。
②能证明该方案可行的实验现象是 _。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三3月教学质量检查理综化学试卷(解析版) 题型:选择题
探究浓硫酸和铜的反应,下列装置或操作正确的是

A.用装置甲进行铜和浓硫酸的反应
B.用装置乙收集二氧化硫并吸收尾气
C.用装置丙稀释反应后的混合液
D.用装置丁测定余酸的浓度
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
关于下列各装置图的叙述不正确的是
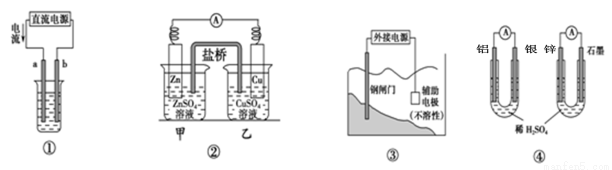
A.用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液
B.图②装置的盐桥中KCl的Cl-移向乙烧杯
C.图③装置中钢闸门应与外接电源的正极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com