
请仔细观察两种电池的构造示意图,

回答下列问题:
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,
则负极的电极反应式: 。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其可能的原因是 。
(3)原电池可将化学能转化为电能。某课外活动小组设计两种类型的原电池,以 探究其能量转化效率。
限选材料:ZnSO4(aq), CuSO4(aq);铜片,锌片和导线。
①完成原电池甲的装置示意图(见下图),并作相应标注。
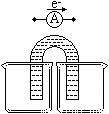
(要求:在同一烧杯中,电极与溶液含相同的金属元素)
②组装原电池乙,要求:以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中,工作一段时间后,可观察到负极 。
③甲乙两种原电池中可更有效地将化学能转化为电能的是 ,(填“甲”或“乙”),其原因是 。
(1)Zn+2OH--2e-=Zn(OH) 2(2)碱性锌锰电池用锌粉替代了原锌锰电池的锌壳,增大了反应物的接触面积,加快了反应速率,故放电电流大。(3)①
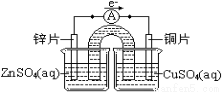
②金属被腐蚀(氧化),表面有红色固体物质生成。
③甲 有盐桥存在时,负极金属与CuSO4(aq)没有直接接触,二者不会发生置换反应,化学能不会转化成热能,几乎全部转化成电能。
【解析】
试题分析:(1)电池是碱性电池,负极是化合价升高,发生氧化反应,因此Zn作负极,先写出Zn-2e-=Zn(OH)2,再根据反应前后原子个数守恒,配平其他,负极电极反应式:Zn+2OH--2e-=Zn(OH)2;(2)从影响反应速率的因素分析,分析两个电池的结构,锌锰电池负极是锌片,而碱性锌锰电池负极是锌粉,锌粉增加了反应物的接触面积,加快了反应速率,使放电电流大幅度提高;(3)①根据题目所给的装置图,得知:左边烧杯是负极,材料是Zn,右边烧杯是正极才,材料是铜片,左烧杯的盛放的溶液是ZnSO4(aq),右边烧杯是CuSO4(aq),因此装置图为: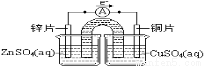 ;
;
②根据原电池的工作原理:锌作负极,Zn-2e-=Zn2+,质量减少,一段时间后锌表面有红色物质生成;③两种原电池原电池甲放电时间较长,因此甲装置更能有效地将化学能转化为电能;有盐桥存在时,负极金属与CuSO4(aq)没有直接接触,二者不会发生置换反应,化学能不会转化成热能,几乎全部转化成电能。
考点:考查原电池的工作原理。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于浓硫酸的叙述正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.稀释浓硫酸时,先将浓硫酸加入烧杯中,再加入水并搅拌
C.浓硫酸是一种干燥剂,能够干燥氨气、氧气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
调查发现,某些新装修的居室中空气污染物浓度过高,对人体健康产生一定影响。这些污染物最常见的是
A.SO2 B.CO2
C.C2H4 D.苯、甲苯、醛类等有机物
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
晒太阳帮助人体钙吸收,其主要原因是阳光照射有助于人体内合成
A.维生素A B.维生素B2 C.维生素C D.维生素D
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
下列哪种物质可用于和氢氧化钠溶液共热后制得肥皂
A.葡萄糖 B.蛋白质 C.油脂 D.乙酸
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
下列现象或反应的原理解释正确的是
选项 | 现象或反应 | 原理解释 |
A | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 |
B | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
C | 镀层破损后,镀锡铁比镀锌铁易腐蚀 | 锡比锌活泼 |
D | 2CO=2C+O2在任何条件下均不能自发进行 | 该反应 △H>0, △S<0 |
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
25 ℃、101 kPa下:①2Na(s)+  O2(g)===Na2O(s);ΔH1=-414 kJ/mol
O2(g)===Na2O(s);ΔH1=-414 kJ/mol
②2Na(s)+O2(g)===Na2O2(s);ΔH2=-511 kJ/mol
下列说法正确的是
A.①和②产物中的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)===2Na2O(s) ; ΔH=-317 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高二上学期第二次月考化学试卷(解析版) 题型:选择题
在t℃下,某反应达到平衡,平衡常数K= 。恒容时,温度升高,NO浓度减小。下列说法正确的是
。恒容时,温度升高,NO浓度减小。下列说法正确的是
A.升高温度,逆反应速率减小
B.该反应化学方程式为:NO+SO3 NO2+SO2
NO2+SO2
C.该反应的焓变为正值
D.K表达式中,C(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,若使混和液pH=7,则酸与碱溶液的体积比是
A.10:1 B.1:10 C.1:2 D.2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com