
| 56x |
| 12y |
| 14 |
| 1 |
| x |
| y |
| 3 |
| 1 |
| ||
| ||


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

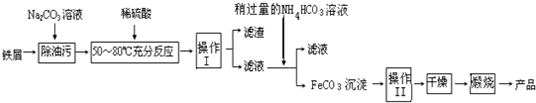
| 实验方案 | 预期现象 | |
| a | 加NaOH溶液 | 产生白色沉淀,变灰绿再变红褐 |
| b | 先加KSCN溶液,再加氯水 | 先无明显现象,后变红 |
| c | 加酸性KMnO4溶液 | 紫色褪去 |
| d | 先加氯水,再加KSCN溶液 | 溶液先变黄,再变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
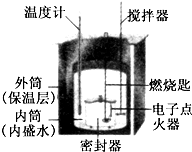 某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.
某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
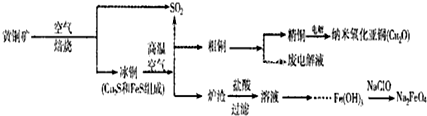
n(SO
| 91:9 | 1:1 | 1:91 | ||||
| PH(25℃) | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
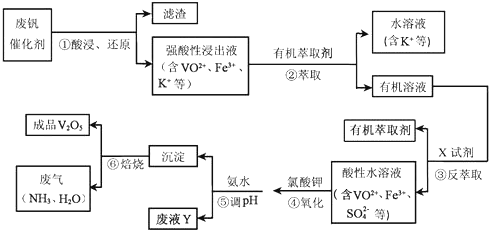
| Ph | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/ | 88 | 92 | 93 | 95 | 95 | 95 | 93 | 90 | 87 |
查看答案和解析>>
科目:高中化学 来源: 题型:
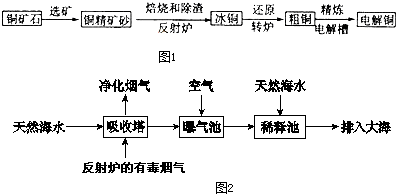
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,可能有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加硝酸银溶液产生白色沉淀,一定有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com