
���û�ѧ��Ӧԭ���о�������ȵ��ʼ��仯����ķ�Ӧ����Ҫ����
 ��1����������������2SO2(g)��O2(g)
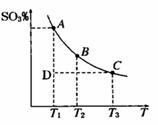
��1����������������2SO2(g)��O2(g) 2SO3(g)��ƽ������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ��������ͼ�ش��������⣺
2SO3(g)��ƽ������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ��������ͼ�ش��������⣺
��2SO2(g)+O2(g) 2SO3(g)�ġ�H__________0���>����<������
2SO3(g)�ġ�H__________0���>����<������
��һ�������£���SO2��O2�������2:1����һ���������ܱ������з������Ϸ�Ӧ����˵���÷�Ӧ�Ѵﵽƽ����� ��
a����ϵ���ܶȲ������仯 b��SO2��SO3������ȱ��ֲ���
c����ϵ����Ԫ�ص������ٷֺ������ٱ仯
d����λʱ����ת��4 mol ���ӣ�ͬʱ����2 mol SO3
e�������ڵ���������������ٱ仯
��2��һ���������£��ϳɰ���ӦΪ��N2(g)+3H2(g)  2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣
2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣
ͼ1 ͼ2 ͼ3
����ͼ2��Ϣ������0~10min�ڸ÷�Ӧ��ƽ������v(H2)= ����11min�������������䣬ѹ�����������Ϊ1L����n(N2)�ı仯����Ϊ (�a����b����c����d��)
��ͼ3 ��a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ��� �㣬�¶�T1 T2���>����=����<����
��3������β����NOx��CO�����ɼ�ת��
����֪����������NO�ķ�ӦΪ��N2(g)+O2(g) 2NO(g) ��H
2NO(g) ��H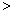 0 ��1mol������0.8molN2��0.2molO2��1300oCʱ���ܱ������ڷ�Ӧ�ﵽƽ�⣬���NOΪ8��10��4mol��������¶��µ�ƽ�ⳣ��K= �����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��
0 ��1mol������0.8molN2��0.2molO2��1300oCʱ���ܱ������ڷ�Ӧ�ﵽƽ�⣬���NOΪ8��10��4mol��������¶��µ�ƽ�ⳣ��K= �����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��
������ȼ�Ͳ���ȫȼ��ʱ����CO���������밴���з�Ӧ��ȥCO��2CO(g)=2C(s)+O2(g) ��֪�÷�Ӧ�ġ�H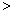 0�������������ܷ�ʵ�ֵ����ݣ� ��
0�������������ܷ�ʵ�ֵ����ݣ� ��
 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ʊ�пӡˢ��·������ϡ���ḯʴп�壬�����ķ�Һ�ơ��ð�Һ�������ð�Һ���к�����п�⣬����������ˮ�����Cl—��Fe3+����ʵ������á��ð�Һ����ȡZnSO4·7H2O�Ĺ������£�

��1����ϡ���ḯʴп��ʱ��ԭ����ΪN2O���������뻹ԭ�������ʵ���֮���� ��
��2��������ٵ�pH>12����Zn(OH)2�ܽ��������ǻ���п���ơ�д��Zn(OH)2���ܽ�����ӷ���ʽ ��
��3����ҺD�г��˺���OH—�����⣬�����е��������� �������ӷ��ţ���
��4������ҺE��pH=4��c(Zn2+)=2mol·L-1��c(Fe3+)=2.6��l0-9mol·L-1������õ��ܶȻ��� ����ѡ���
A.Ksp[Zn(OH)2] B.Ksp[Zn(OH)2]��Ksp[Fe(OH)3] C.Ksp[Fe(OH)3]
��5�������Ҫ����pH��һ����Χ��ʵ������pH��ֽ�ⶨ��ҺpH�ķ����ǣ� ���� ��
��6����֪����Fe(OH)3(s) Fe3+(aq)+3OH-(aq) �� ��H= a kJ•mol-1
Fe3+(aq)+3OH-(aq) �� ��H= a kJ•mol-1
��H2O(l)  H+(aq)+OH-(aq) ����H= b kJ•mol-1
H+(aq)+OH-(aq) ����H= b kJ•mol-1
��д��Fe3+����ˮ�ⷴӦ���Ȼ�ѧ����ʽ�� ��
���ٵ��ܶȻ�����ΪKSP���ڵ����ӻ�����ΪKW��Fe3+����ˮ�ⷴӦ��ƽ�ⳣ����
K= �����ú�KSP��KW�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�� CH3CH2OH  CH2=CH2��+H20
CH2=CH2��+H20
CH2=CH2+Br2  BrCH2��CH2Br
BrCH2��CH2Br
���Ҵ���1,2-�������顢���ѵ��й������������±���ʾ��
�Ҵ� | 1,2-�������� | ���� | |
ͨ��״���µ�״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/g��cm-3 | 0.79 | 2.2 | 0.71 |
�۵�/�� | -130 | 9 | -116 |
�е�/�� | 78.5 | 132 | 34.6 |
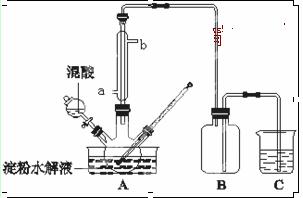
 ij��ѧС�������Ҵ������Ϊԭ����ʵ�����Ʊ�������1,2һ�������飬ʵ��װ������ͼ��ʾ(װ��A�еļ��Ȳ��ֵ�����װ��ʡ��û�л���)��
ij��ѧС�������Ҵ������Ϊԭ����ʵ�����Ʊ�������1,2һ�������飬ʵ��װ������ͼ��ʾ(װ��A�еļ��Ȳ��ֵ�����װ��ʡ��û�л���)��
��1������E�������� ��
��2����������©�������IJ����ܵ��� ���� (����ĸ)��
a��ʹ©����Һ��������
b��������������������
c����ֹA��������ƿ���Һ�屬��
��3��ʵ��ʱ��A��������ƿ����뼸Ƭ���Ƭ��Ŀ���� �����ȷ�Ӧ�����У�������ƿ���������ϩ�⣬���������ɵ��л���������Ҫ�� ��
��4����Ӧ�����У���B�г���������(��)���Һ����������˵������������ (�D�г��ֶ�������C�������ѳ�����)��ɵġ�
��5����Ӧ�����У�D��������ˮ��ȴʢ��Һ����Թܣ�����ҪĿ���� ��
˵���Ʊ�1,2-��������ķ�Ӧ�Ѿ�������ʵ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪��B������C��Hԭ�Ӹ�����Ϊ1�U2����Է�������Ϊ28���˴Ź���������ʾ������ֻ��һ�ֻ�ѧ��������ԭ�ӣ��������µ�ת����ϵ��
��֪��B������C��Hԭ�Ӹ�����Ϊ1�U2����Է�������Ϊ28���˴Ź���������ʾ������ֻ��һ�ֻ�ѧ��������ԭ�ӣ��������µ�ת����ϵ��
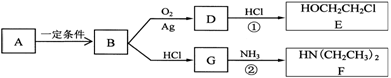
��1��B�Ľṹ��ʽ��
��2����Ӧ����D��HCl�����ʵ���֮��1�U1�Ļ��Ϸ�Ӧ����D�ķ���ʽ��
��Ӧ�ڿɱ�ʾΪ��G + NH3 �� F + HCl (δ��ƽ)���÷�Ӧ��ƽ��Ļ�ѧ����ʽ�ǣ��л���������ýṹ��ʽ��ʾ����
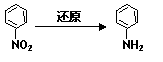 ������E��HOCH2CH2Cl���� F [ HN(CH2CH3)2 ]��ҩƷ��³����ϳɵ���Ҫ�м��壬��³����ĺϳ�·�����£�����֪�� ��
������E��HOCH2CH2Cl���� F [ HN(CH2CH3)2 ]��ҩƷ��³����ϳɵ���Ҫ�м��壬��³����ĺϳ�·�����£�����֪�� ��
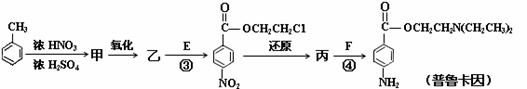
��3���Ľṹ��ʽ�� ���ɼױ����ɼķ�Ӧ������ ��1�֣�
��4�����������ֺ��������ţ���Ӧ�۵Ļ�ѧ����ʽ�ǣ�
��5����³����������ˮ����ﶡ����
�������Ϊͬ���칹�壬��Ľṹ��ʽ��
���쾭�ۺϷ�Ӧ�Ƴɵĸ߷�����ά�㷺����ͨѶ��������þۺϷ�Ӧ�Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
t��ʱ��ˮ�����ӻ�ΪKW���ڸ��¶��£���Ͽ����Ե�һԪ��HA��һԪ��BOH����Һ�������йػ��Һ�ĸ��ֹ�ϵ�У���ȷ�ϻ��Һ�����Ե���
A��pH=7 B��c(OH��)��
C��c(A��) > c(B+) D��c(H+)��c(OH��)��c(A��)��c(B+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��2M(g) N(g)����H <0���ֽ�M��N�Ļ������ͨ�����Ϊ1L�ĺ����ܱ�����
N(g)����H <0���ֽ�M��N�Ļ������ͨ�����Ϊ1L�ĺ����ܱ�����
 �У���Ӧ��ϵ������Ũ����ʱ��仯��ϵ����ͼ��ʾ������˵����ȷ���ǣ� ��
�У���Ӧ��ϵ������Ũ����ʱ��仯��ϵ����ͼ��ʾ������˵����ȷ���ǣ� ��

 A��a��b��c��d�ĸ����д���ƽ��״̬�ĵ���a��b
A��a��b��c��d�ĸ����д���ƽ��״̬�ĵ���a��b
 B����Ӧ������25minʱ�����߷����仯��ԭ���Ǽ���
B����Ӧ������25minʱ�����߷����仯��ԭ���Ǽ��� �� 0.4molN
�� 0.4molN
 C���������¶�ʹ35minʱ��ϵ��N�İٷֺ�����
C���������¶�ʹ35minʱ��ϵ��N�İٷֺ����� 15minʱ��ȣ�Ӧ�����¶�
15minʱ��ȣ�Ӧ�����¶�
 D����40min�������ͼ��ʾ�仯��������Ǽ�����
D����40min�������ͼ��ʾ�仯��������Ǽ����� ij�ִ���
ij�ִ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ���� �� ��
A��NH4HCO3��Һ�����NaOH��Һ��Ӧ��NH 4++ OH�D��NH3��+ H2O
B���ö��Ե缫��ⱥ���Ȼ�����Һ��2Cl�D + 2H +  H2��+ Cl2��
H2��+ Cl2��
C����Fe��NO3��3��Һ�м��������HI��Һ��2Fe3++2I�D �� 2Fe2++I2
D��Na2SO3��Һʹ����KMnO4��Һ��ɫ��5SO32�D + 6H+ + 2MnO4�D��5SO4 2�D + 2Mn2+ +3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ��װ���ܴﵽʵ��Ŀ�ĵ���(�г�����δ����)

A����װ�����ڼ���1-�������ȥ���� B����װ������ʯ�͵ķ���
C����װ������ʵ������������ D����װ�ÿ�֤�����ԣ����̼�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com