
| A、①②④⑤ | B、①②⑤⑦ |
| C、①②⑤⑥ | D、②⑤⑥⑦ |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |


科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁粉和氯化铁溶液反应 Fe+2Fe3+→3Fe2+ |
| B、铁和稀盐酸反应 2Fe+6H+→2Fe3++H2↑ |
| C、硫化亚铁溶于稀硝酸中:FeS+2H+→Fe2++H2S↑ |
| D、铝和氢氧化钠溶液反应 2Al+2OH-→2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、① | B、② | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定达终点时,俯视读数 |
| B、碱液移入锥形瓶后,加入10mL蒸馏水 |
| C、酸式滴定管用蒸馏水洗涤后,未用标准液润洗 |
| D、滴定振荡锥形瓶过程中,有少量溶液溅出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 官能团名称 | 羧基 | 醛基 | 羟基 | 氨基 |
| 结构简式 | -COOH | -COH | OH- | -NH3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
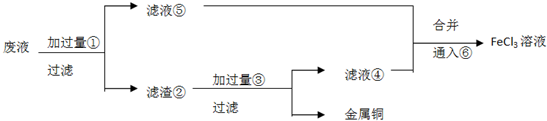
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com