
A、ρ=
| ||
B、ω=
| ||
C、ω=
| ||
D、c=
|
| 溶液质量 |
| 氨气体积 |
| 1000ρω |
| M |
| V |
| Vm |
| 氨气质量 |
| 溶液质量 |
| 溶质物质的量 |
| 氨气体积+水的体积 |
| 溶液质量 |
| 氨气体积 |
| 1000ρω |
| M |
| 17c |
| 1000ρ |
| VL |
| 22.4L/mol |
| V |
| 22.4 |
| V |
| 22.4 |
| 17V |
| 22.4 |
| ||
|
| 17V |
| 17V+22400 |
| 溶质物质的量 |
| 氨气体积+水的体积 |


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
A、c=
| ||
B、p=m+
| ||
| C、n=m+0.017Vc | ||
D、n=p+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、200mL |
| B、245mL |
| C、250mL |
| D、300mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 时刻 | 时间 | 可能采取的措施 | 体系中平衡移动的方向 |
| 3 | - | ---- | |
| - | 3~4 | ---- | |
| 5 | - | ---- | |
| - | 5~6 | ---- | |
| 7 | - | ---- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3 |
| B、NaHCO3 |
| C、Na2CO3和NaOH |
| D、Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
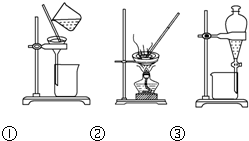
| A、洗涤沉淀时(如图①),向漏斗中加适量水,搅拌并滤干 | ||
| B、用CCl4提取碘水中的碘,选③ | ||
C、蒸馏时蒸馏烧瓶中液体的体积不能超过容积的
| ||
| D、粗盐提纯,选①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3OH |
| B、C2H5OH |
| C、C3H7OH |
| D、C4H9OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①②③ | D、①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com