
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。 (1)T业上用黄铁矿(FeS2)在高温下和氧气反应制备SO2:4FeS2+11O2 8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
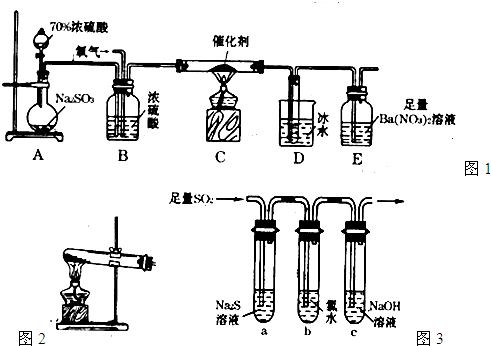
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率(已知SO3。熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)。

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______。
②当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______。
③实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简)。
(3)某兴趣小组欲在绿色环保的条件下探究SO2的性质,设计如下图实验装置。

B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为_______;
C中反应的离子方程式为______ ;D中的实验现象为______ ;E装置的作用是______。
(1)S、Fe 11.2
(2)①打分液漏斗上的活塞,旋开分液漏斗的旋塞,缓慢滴加。②使残留在装置中的二氧化硫和三氧化硫被充分吸收。③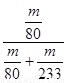 ×100﹪
×100﹪
(3)品红溶液 SO2+I2+2H2O=SO42-+2I-+4H+ 试管中有淡黄色沉淀生成。 吸收尾气,防止倒吸。
【解析】
试题分析:在反应4FeS2+11O2 8SO2+2Fe2O3中FeS2中的Fe为+2价,反应后变为Fe2O3的+3价,化合价升高,失去电子,被氧化;FeS2中的S为-1价,反应后变为SO2的+4价,化合价升高,失去电子,被氧化. 该反应中被氧化的元素是Fe、S。在该反应中每产生8mol的SO2转移电子44mol. 。现在转移2. 75mol电子,所以产生SO2在标准状况下的体积为(2. 75mol÷44mol)×8mol×22.4L/mol=11.2L. (2) ①使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是打分液漏斗上的活塞,旋开分液漏斗的旋塞,缓慢滴加。②当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是使残留在装置中的二氧化硫和三氧化硫被充分吸收。③装置D中增加的质量是SO3的质量,E中的沉淀为BaSO4。则此条件下二氧化硫的转化率是
8SO2+2Fe2O3中FeS2中的Fe为+2价,反应后变为Fe2O3的+3价,化合价升高,失去电子,被氧化;FeS2中的S为-1价,反应后变为SO2的+4价,化合价升高,失去电子,被氧化. 该反应中被氧化的元素是Fe、S。在该反应中每产生8mol的SO2转移电子44mol. 。现在转移2. 75mol电子,所以产生SO2在标准状况下的体积为(2. 75mol÷44mol)×8mol×22.4L/mol=11.2L. (2) ①使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是打分液漏斗上的活塞,旋开分液漏斗的旋塞,缓慢滴加。②当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是使残留在装置中的二氧化硫和三氧化硫被充分吸收。③装置D中增加的质量是SO3的质量,E中的沉淀为BaSO4。则此条件下二氧化硫的转化率是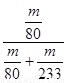 ×100﹪。(3) B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液,C中反应的离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+,D中发生的反应为:SO2+2H2S=3S↓+2H2O。产生的S是不溶于水的淡黄色沉淀。故D的实验现象为试管中有淡黄色沉淀生成。SO2是有害的气体,容易导致大气污染,是大气污染物,E装置的作用是既能吸收尾气,也能防止倒吸现象的发生。
×100﹪。(3) B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液,C中反应的离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+,D中发生的反应为:SO2+2H2S=3S↓+2H2O。产生的S是不溶于水的淡黄色沉淀。故D的实验现象为试管中有淡黄色沉淀生成。SO2是有害的气体,容易导致大气污染,是大气污染物,E装置的作用是既能吸收尾气,也能防止倒吸现象的发生。
考点:考查SO2的制备方法和性质的知识。


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| △ |
| ||
| △ |
| ||||
|
| ||||
|
查看答案和解析>>
科目:高中化学 来源:2013届天津市天津一中高三第四次月考化学试卷(带解析) 题型:实验题
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2: ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16. 8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。) 
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是 。
②实验过程中,需要通入氧气。试写出一个用右图所示装置制取氧气的化学方程式 。
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是 。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如右图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验: 
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)= (用含硫微粒浓度的代数式表示)。)】
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市河北区高三年级总复习质量检测二理综化学试卷(解析版) 题型:实验题
I、二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。

(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
 ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。
(2)一化学研究性学习小组设计用如下装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaC!:溶液,产生白色沉淀上述方案合理的是方案______(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子反应方程式为____________________。
③当通入二氧化硫至试管c中溶液显中性时,溶液中c(Na+)=________________(用含硫元素微粒浓度的代数式表示)。
Ⅱ、另一化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:
电解时,粗铜应与电源的______极相连。阴极上的电极反应式为____________。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市高三第四次月考化学试卷(解析版) 题型:实验题
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
 ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16. 8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是 。
②实验过程中,需要通入氧气。试写出一个用右图所示装置制取氧气的化学方程式 。

③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是 。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如右图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:

方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)= (用含硫微粒浓度的代数式表示)。)】
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com