
【题目】(1)硫元素位于元素周期表第____列;硫元素原子核外有2个未成对电子,这2个电子所处亚层的符号是_______;硫、氯元素的原子均可形成与Ar原子电子层结构相同的简单离子,且硫离子的半径更大,请解释__________________。
(2)S8和P4的分子中都只有共价单键,若P4分子中有6个P-P键,则可推断S8分子有___个S-S键;已知:H-S键键能:339 kJ/mol;H-Se键键能:314 kJ/mol。以上键能数据能否比较S、Se非金属性的强弱______(选填“能”、“否”;下同);能否比较H2S、H2Se沸点的高低______。
(3)在25℃,Na2SO3溶液吸收SO2得到的NaHSO3溶液中c(SO32-)>c (H2SO3),据此判断NaHSO3溶液显___性。
(4)在25℃,Na2SO3溶液吸收SO2后,若溶液pH=7.2,则溶液中c(SO32-)=c (HSO3-);若溶液pH=7,则以下浓度关系正确的是(选填编号)___________。
a.c(Na+) = 2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
(5)已知Na2SO3溶液中存在水解平衡:SO32-+H2O![]() HSO3-+OH-,请用Na2SO3溶液和a试剂及必要的实验用品,设计简单实验,证明盐类的水解是一个吸热过程。a试剂是__________,操作和现象是__________________。
HSO3-+OH-,请用Na2SO3溶液和a试剂及必要的实验用品,设计简单实验,证明盐类的水解是一个吸热过程。a试剂是__________,操作和现象是__________________。
【答案】 16 3p 氯离子核电荷数更大,对外层电子的引力更强,故离子半径较硫离子小。 8 能 否 酸 ab 酚酞 取样品溶于水,滴加酚酞显红色,加热后溶液红色加深
【解析】(1)硫元素位于元素周期表第16列;硫元素原子核外有2个未成对电子,这2个电子所处亚层的符号是3p;由于氯离子核电荷数更大,对外层电子的引力更强,故离子半径较硫离子小。(2)因为S8的分子中都只有共价单键,所以结构模型为![]() ,所以S8分子有8个S-S键;共价键的键能越大氢化物越稳定,中心元素的非金属性越强,H2S、H2Se沸点的高低无键能的大小无关,与分子间作用力的大小有关。(3)在25℃,Na2SO3溶液吸收SO2得到的NaHSO3溶液中c(SO32-)>c (H2SO3),这说明亚硫酸氢根的电离程度大于水解程度,NaHSO3溶液显酸性。(4)a.溶液pH=7,溶液显中性,根据电荷守恒c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)可知c(Na+) = 2c(SO32-)+c(HSO3-),a正确;b.亚硫酸氢根的电离程度或水解程度均较小,则溶液中c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-),b正确;c.根据电荷守恒c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)可知c错误,答案选ab;(5)已知Na2SO3溶液中存在水解平衡:SO32-+H2O
,所以S8分子有8个S-S键;共价键的键能越大氢化物越稳定,中心元素的非金属性越强,H2S、H2Se沸点的高低无键能的大小无关,与分子间作用力的大小有关。(3)在25℃,Na2SO3溶液吸收SO2得到的NaHSO3溶液中c(SO32-)>c (H2SO3),这说明亚硫酸氢根的电离程度大于水解程度,NaHSO3溶液显酸性。(4)a.溶液pH=7,溶液显中性,根据电荷守恒c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)可知c(Na+) = 2c(SO32-)+c(HSO3-),a正确;b.亚硫酸氢根的电离程度或水解程度均较小,则溶液中c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-),b正确;c.根据电荷守恒c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)可知c错误,答案选ab;(5)已知Na2SO3溶液中存在水解平衡:SO32-+H2O![]() HSO3-+OH-,即水解溶液显碱性,因此可以用酚酞试液检验,操作和现象是:取样品溶于水,滴加酚酞显红色,加热后溶液红色加深,说明水解吸热。
HSO3-+OH-,即水解溶液显碱性,因此可以用酚酞试液检验,操作和现象是:取样品溶于水,滴加酚酞显红色,加热后溶液红色加深,说明水解吸热。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2
B. 苯的结构简式为![]() ,能使酸性高锰酸钾溶液褪色
,能使酸性高锰酸钾溶液褪色
C. 相同物质的量的乙烯与乙醇分别在足量的O2中完全燃烧,消耗O2的物质的量相同
D. 乙烯和植物油都能使溴水褪色,其褪色原理不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用11.92gNaClO配成100mL溶液,向其中加入0.01mol Na2Sx恰好完全反应,生成Na2SO4和NaCl。
(1)NaClO溶液的物质的量浓度_________mol·L-1。
(2)化学式Na2Sx中的X=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物命名及其一氯代物的同分异构体数目正确的是
命名 | 一氯代物 | |
A | 2-甲基-2-乙基丙烷 | 4 |
B | 1,3-二甲基苯 | 3 |
C | 2,2,3-三甲基戊烷 | 6 |
D | 2,3 -二甲基- 4-乙基己烷 | 7 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是( )
2CO(g),达到平衡状态的标志是( )
①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态
A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学上对血液中毒最常用的净化手段是血液透析。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透。血液中的蛋白质和血细胞不能透过透析膜,血液内的毒性物质则可以通过,由此可以判断( )
A.蛋白质、血细胞不溶于水,毒性物质可溶于水
B.蛋白质以分子形式存在,毒性物质以离子形式存在
C.蛋白质、血细胞的粒子直径大于毒性物质的粒子直径
D.蛋白质、血细胞不能透过滤纸,毒性物质能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于分散系和胶体的说法正确的是( )
A.胶体、溶液、浊液都是分散系 B.分散质粒子的半径:浊液>溶液>胶体
C.可见光通过溶液时,产生丁达尔现象 D.胶体都不透明,且稳定性极强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校活动小组的同学拟用乙烯催化还原二氧化硫的方法来制取单质硫。
(1)甲组同学用乙醇脱水的反应来制取纯净的乙烯气体,其反应原理及制备装置如下:
主反应:C2H5OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
副反应:C2H5OH+2H2SO4(浓) ![]() C+2SO2↑+5H2O;
C+2SO2↑+5H2O;
C+H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
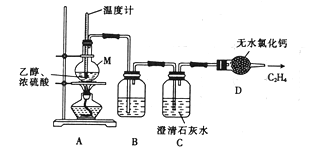
① 仪器M的名称是_______________。
② 装置B 中盛放的试剂可能是____________。
③ 装置C 的作用是______________
(2)乙组同学用甲组同学制得的乙烯并结合下列装置进行乙烯催化还原二氧化硫的实验。
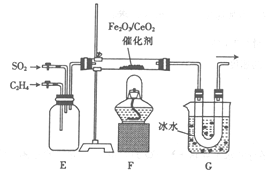
① 装置E的作用是___________;装置G的作用是_____________。
② 玻璃管中有硫及二氧化碳生成,该反应的化学方程式为_________。
③ 用下列装置检验G中逸出的气体含有氧化产物CO2。
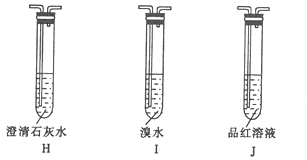
装置正确的连接顺序为G![]() _________,证明G中逸出的气体含有CO2的现象为_______。
_________,证明G中逸出的气体含有CO2的现象为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com