
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.两原子的核外电子排布相同,则一定属于同种元素 |
| D.一种阳离子和一种阴离子的质子数和电子数可能同时相等 |
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:填空题
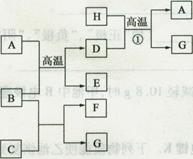

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
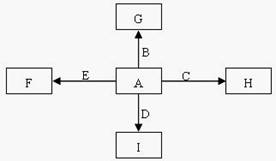
 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;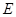 可以发生反应:2E+I
可以发生反应:2E+I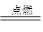 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第9列中元素中没有非金属元素 |
| B.只有第二列的元素原子最外层电子排布为ns2 |
| C.第四周期第9列元素是铁元素 |
| D.第10、11列为ds区 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电负性用来描述不同元素的原子对键合电子吸引力的大小 |
| B.电负性是以氟为4.0、锂为1.0作为标准的相对值 |
| C.元素电负性越小,元素金属性越强 |
| D.元素电负性越大,元素非金属性越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 元素化合价判断丙、丁是否在一定条件下生成单质D,简述判断理由。
元素化合价判断丙、丁是否在一定条件下生成单质D,简述判断理由。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com