
| A.18.4g | B.13.8g | C.8.2g | D.9.2g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
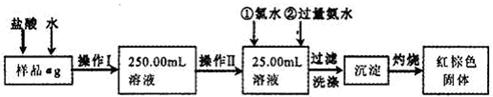
| A.50mL烧杯 | B.50mL量筒 | C.25mL碱式滴定管 | D.25mL酸式滴定管 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应中氧化剂与还原剂物质的量之比为1︰8 |
| B.若有lmol NO3— 发生还原反应,转移电子数为5mol |
| C.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| D.若把该反应设计成原电池,负极反应为Fe2+—e— =Fe 3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合粉末的质量为3.2g |
| B.混合粉末中CuO和Fe2O3的物质的量相等 |
| C.混合粉末中CuO 和Fe2O3的质量相等 |
| D.混合粉末溶于硝酸所得溶液中c( NO3-)为0.5 mo/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 g | B.2.8 g | C.14 g | D.8.4 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在潮湿的空气中放置不易生锈 | B.硬度比生铁大 |
| C.与2mol/L盐酸的反应生成氢气 | D.在冷的浓H2SO4溶液中可钝化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com