
常温下,下列关于电解质溶液的判断正确的是( )
A.在PH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在PH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.0.1mol/L一元碱BOH溶液的PH=10,可推知BOH溶液中存在BOH = B+ + OH-
D.在0.1mol/L一元酸HA溶液的PH=3,可推知NaA溶液中存在:A- + H2O HA + OH-
HA + OH-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
密闭容器中,反应xA(g)+yB(g)=zC(g)达平衡时,A的浓度为0.5mol/L,
若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L.下列判断正确的是
A.x+y<z B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组化合物中,化学键类型有关叙述正确的是( )
A.CaCl2和Na2O2中都只含有离子键
B.NaOH和NaHS都既含有离子键,又含有极性键
C.CO2和H2S中都只含有非极性键
D.H2O2和CS2都既含有极性键,又含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
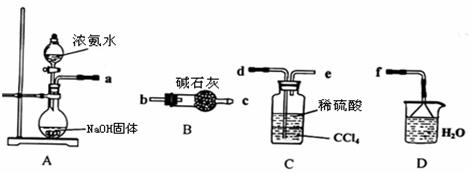
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:
。
(3)将装置C中两种液体分离开的操作名称是 。
(4)(NH4)2SO4“低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意 。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
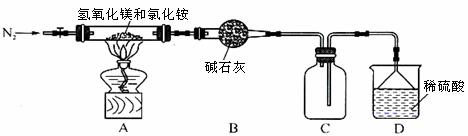
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 。
(2)反应过程中持续通入N2的作用是 。
(3)由MgCl2溶液蒸发得到MgCl2·6H2O晶体,蒸发的目的是_________。
a.得到热饱和溶液 b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:
。
②由MgCl2·6H2O制备无水MgCl2的操作在 氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
查看答案和解析>>
科目:高中化学 来源: 题型:
将H2(g)和I2(g)充入恒容密闭容器中,恒温下发生反应:H2(g) + I2(g)  2HI(g) ,△H<0,平衡时,I2(g)的转化率为a;若初始条件相同,绝热下发生上述反应,平衡时,I2(g)的转化率为b。则a与b的关系是( )
2HI(g) ,△H<0,平衡时,I2(g)的转化率为a;若初始条件相同,绝热下发生上述反应,平衡时,I2(g)的转化率为b。则a与b的关系是( )
A.a>b B.a=b C.a<b D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,测得0.01mol/L NaOH溶液的PH为11,则该温度下,水的离子积Kw=_____________。在此温度下,将PH= a 的NaOH溶液Va L与PH= b 的硫酸Vb L混合。
①若所得溶液为中性,且a=12,b=2,则Va :Vb = __________________________
②若所得混合液的PH=10,且a=12,b=2,则Va :Vb = ______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
将铁片和银片用导线连接置于同一稀盐酸溶液中,并经过一段时间后,下列叙述正确的
A.负极有Cl2逸出,正极有H2逸出 B.负极附近Cl-的浓度减小
C.正极附近Cl-的浓度逐渐增大 D.溶液中Cl-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 除去Fe2O3中的少量Al2O3 | 向混合物中滴加足量NaOH溶液,过滤 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸,过滤 |
| C | 证明钠的金属活动性比铝强 | 向AlCl3溶液中投入金属钠 |
| D | 实验室制备Al(OH)3 | 向Al2(SO4)3溶液中加入足量NaOH溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同。回答下列问题:

(1)左边大试管中要加入几片碎瓷片,其作用是
__________________________________;
(2)该装置中使用的玻璃导管较长,其作用是
____________________________________;
(3)烧杯中还要盛有的物质是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com