
铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
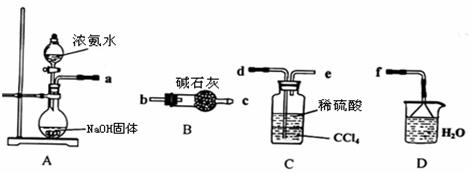
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:
。
(3)将装置C中两种液体分离开的操作名称是 。
(4)(NH4)2SO4“低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意 。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
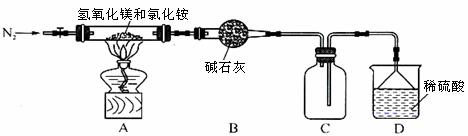
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 。
(2)反应过程中持续通入N2的作用是 。
(3)由MgCl2溶液蒸发得到MgCl2·6H2O晶体,蒸发的目的是_________。
a.得到热饱和溶液 b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:
。
②由MgCl2·6H2O制备无水MgCl2的操作在 氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
Ⅰ(1)d e f (2分)
(2)氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡NH3+H2O  NH4++OH—左移,有利氨气逸出。(2分)
NH4++OH—左移,有利氨气逸出。(2分)
(3) 分液(2分);吸收多余的NH3防止污染空气,防止倒吸(2分)
(4)密封、阴凉、通风(2分)
Ⅱ(1)Mg(OH)2+NH4Cl MgOHCl+NH3↑+H2O(2分) 干燥氨气(2分)
MgOHCl+NH3↑+H2O(2分) 干燥氨气(2分)
(2)使反应产生的氨气完全导出并被稀硫酸充分吸收,(2分)
(3)a(2分)
(4)①用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。(2分)(答焰色反应也给分)
②HCl(气流)(2分)


科目:高中化学 来源: 题型:
(1)pH=13的CH3COONa溶液加水稀释100倍后,pH________11(填“>”“=”或“<”)原因是______________________________________________(用离子方程式和必要的文字说明);pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH________NaOH溶液的pH(填“>”“=”或“<”);
(2)pH相等时,①NH4Cl ②(NH4)2SO4 ③NH4HSO4三种溶液中c(NH )由大到小的顺序为________;
)由大到小的顺序为________;
(3)等体积、等浓度的氢氧化钠与醋酸混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)(填“>”“=”或“<”);
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c(NH )=c(Cl-),则混合后溶液呈________性,盐酸的体积________氨水的体积(填“>”“=”或“<”);
)=c(Cl-),则混合后溶液呈________性,盐酸的体积________氨水的体积(填“>”“=”或“<”);
(5)NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO 。该溶液中c(H+)_________________________c(OH-)+c(SO
。该溶液中c(H+)_________________________c(OH-)+c(SO )(填“>”“=”或“<”)。
)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
为纪念编制了第一个元素周期表的俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。下列关于了258Md和260Md的叙述正确的是
A.258Md原子所含中子数与质子数之差为56
B.258Md和260Md互称为同素异形体
C.258Md和260Md为同一种核素
D.有一种Md元素的相对原子质量为258
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E都是短周期元素,原子序数逐渐增大,原子半径按B、A、E、D、C依次增大。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是__________
(2)甲物质的电子式是________ __
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中反应的离子方程式是
(4)用电子式表示A的气态氢化物的形成过程
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法中正确的是
A.标准状况下,11.2L Cl2和H2混合气体原子数为2NA
B.常温下,pH=1的H2SO4溶液中含有的H+的数目为0.2NA
C.在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA
D.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:CO(g)  C(s) +
C(s) +  O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
A.低温下是自发变化
B.高温下是自发变化
C.低温下是非自发变化,高温下是自发变化
D.任何温度下都是非自发变化
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列关于电解质溶液的判断正确的是( )
A.在PH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在PH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.0.1mol/L一元碱BOH溶液的PH=10,可推知BOH溶液中存在BOH = B+ + OH-
D.在0.1mol/L一元酸HA溶液的PH=3,可推知NaA溶液中存在:A- + H2O HA + OH-
HA + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
| 选项 | A | B | C | D |
| 物质 | MgCl2 | CO2 | HCl | NaOH |
| 所含化学 键类型 | 离子键、 共价键 | 共价键 | 离子键 | 离子键、 共价键 |
| 所属化合 物类型 | 离子 化合物 | 共价 化合物 | 离子 化合物 | 共价 化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com