
为纪念编制了第一个元素周期表的俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。下列关于了258Md和260Md的叙述正确的是
A.258Md原子所含中子数与质子数之差为56
B.258Md和260Md互称为同素异形体
C.258Md和260Md为同一种核素
D.有一种Md元素的相对原子质量为258
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是( )
A.气态氢化物的稳定性: HX<H2Y<ZH3 B.非金属活泼性:Y<X<Z
C.原子半径:X>Y>Z D.原子最外电子层上电子数的关系:2Y= (X+Z)
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中,反应xA(g)+yB(g)=zC(g)达平衡时,A的浓度为0.5mol/L,
若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L.下列判断正确的是
A.x+y<z B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应A + B = C + D 在低温下能自发进行,在高温下不能自发进行,对该反应过程
△H、△S的判断正确的是
A.△H <0 △S <0 B.△H >0 △S >0
C.△H <0 △S >0 D.△H >0 △S <0
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g) + bB(g)  cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。

试比较下列大小关系:T1 ▲ T2, P1 ▲ P2, ΔH ▲ 0,
ΔS ▲ 0。 使用催化剂的是 ▲ 反应线。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①元素原子的最外层电子数等于元素的最高化合价
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③所有元素的原子最外层最多可容纳的电子数均为8
④第三周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
A. ①②③④⑤ B. ①②③ C. ④⑤ D. ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组化合物中,化学键类型有关叙述正确的是( )
A.CaCl2和Na2O2中都只含有离子键
B.NaOH和NaHS都既含有离子键,又含有极性键
C.CO2和H2S中都只含有非极性键
D.H2O2和CS2都既含有极性键,又含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
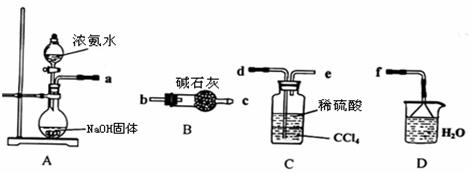
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:
。
(3)将装置C中两种液体分离开的操作名称是 。
(4)(NH4)2SO4“低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意 。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
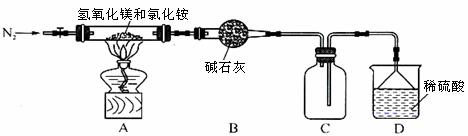
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 。
(2)反应过程中持续通入N2的作用是 。
(3)由MgCl2溶液蒸发得到MgCl2·6H2O晶体,蒸发的目的是_________。
a.得到热饱和溶液 b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:
。
②由MgCl2·6H2O制备无水MgCl2的操作在 氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 除去Fe2O3中的少量Al2O3 | 向混合物中滴加足量NaOH溶液,过滤 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸,过滤 |
| C | 证明钠的金属活动性比铝强 | 向AlCl3溶液中投入金属钠 |
| D | 实验室制备Al(OH)3 | 向Al2(SO4)3溶液中加入足量NaOH溶液,过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com