
分析 (1)高锰酸根离子(MnO4-)反应后的产物与溶液的酸碱性有关;
(2)根据H2C2O4→CO2↑,C化合价升高,则H2C2O4表现还原性并且呈酸性,高锰酸根离子被还原的产物应为Mn2+,据此写出反应的离子方程式;
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色,说明是PbO2将MnSO4氧化成紫红色的高锰酸钾溶液,根据氧化还原反应中,氧化剂和还原剂的强弱判断规律来回答;
(4)①KMnO4与H2O2反应,有气体产生,说明有氧气,溶液褪色说明KMnO4被还原,再根据电子得失守恒和电荷守恒可写出离子方程式;
②根据KMnO4与H2O2反应的物质的量之比求得H2O2的物质的量,进而求得溶液a中c(H2O2);
③由2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,Mn元素化合价从+7降低到+2,据此计算.
解答 解:(1)由不同条件下高锰酸钾可发生的反应可知,溶液的酸性越强,反应后锰元素的化合价越低,所以高锰酸根离子(MnO-4)反应后的产物与溶液的酸碱性有关,
故答案为:溶液酸碱性;
(2)H2C2O4→CO2↑,C化合价升高,则H2C2O4表现还原性并且呈酸性,高锰酸根离子被还原的产物应为Mn2+,即发生还原反应的离子反应过程为MnO4-→Mn2+,所以反应的离子方程式为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,故答案为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O;
(3)将PbO2投入到酸性溶液中搅拌,溶液变为紫红色,证明二者之间发生氧化还原反应生成了高锰酸钾溶液,二氧化铅是氧化剂,硫酸锰是还原剂,
a.氧化剂的氧化性强于氧化产物的氧化性,即氧化性:PbO2>KMnO4,故a正确;
b.还原剂的还原性强于还原产物的还原性,即还原性:MnSO4>PbO2,得不出还原性:PbO2>KMnO4,故b错误;
c、盐酸具有酸性且Cl-具有还原性,PbO2能将Cl-氧化,所以该反应不能用盐酸酸化,故c错误;
d.二氧化铅是氧化剂,则PbO2发生还原反应生成PbSO4,反应式为:PbO2+SO42-+4H++2e-═PbSO4+2H2O,故d正确;
故选ad;
(4)①KMnO4与H2O2反应,有气体产生,说明有氧气,溶液褪色说明KMnO4被还原,再根据电子得失守恒和电荷守恒可写出离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;
故答案为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;
②根据KMnO4与H2O2反应的离子方程式可知关系式为:
2MnO4-~5H2O2
2mol 5mol
0.03mol•L-1×0.02L n(H2O2)
则n(H2O2)=1.5×10-3mol
所以c(H2O2)=$\frac{1.5×10{\;}^{-3}mol}{1.5×10{\;}^{-2}L}$=0.1mol/L
故答案为:0.1mol/L;
③由2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,Mn元素化合价从+7降低到+2,所以反应中转移电子数目0.03mol•L-1×0.02L×(7-2)
=0.003mol,故答案为:0.003.
点评 本题考查氧化还原反应的概念判断和相关计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意从元素化合价的角度认识相关概念并进行计算,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
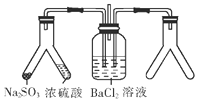
| A. | 大理石和稀盐酸 | B. | CaO和浓氨水 | C. | Cu和浓硝酸 | D. | MnO2和双氧水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 硫具有还原性,可用硫粉覆盖地上洒落的汞 | |
| D. | 硅是重要的半导体材料,常用于制作光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH═CH-CHO | B. |  | ||
| C. | HOCH2-CH2-CH═CH-CHO | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在容积一定温度一定的密闭容器中发生反应M2(?)+2R2(g)?M2R4(g),加入1mol M2和2molR2,反应过程中测得气体的平均相对分子质量随时间的变化如图所示.则下列说法错误的是( )
在容积一定温度一定的密闭容器中发生反应M2(?)+2R2(g)?M2R4(g),加入1mol M2和2molR2,反应过程中测得气体的平均相对分子质量随时间的变化如图所示.则下列说法错误的是( )| A. | M2既可能为固体,也可能为气体 | |
| B. | 达到平衡后,保持容器容枳和温度不变,再加入1molM2和2molR2,则R2转化率不变 | |
| C. | 达到平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,R2的浓度可能是原平衡时的1.8倍 | |
| D. | 若M2为气体,达到平衡后,保持容器容积和温度不变,再加入1molM2R4,则新的平衡时气体的平均相对分子质量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl NaHSO4 KHCO3 | B. | Na2SO4 BaCl2 Na2CO3 | ||
| C. | NaHCO3 Ba(OH)2 NaHSO4 | D. | Ca(OH)2 Na2CO3 BaCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com