
科目:高中化学 来源: 题型:
0.5体积某气态烃只能与0.5体积氯气发生加成反应,生成氯代烷。0.5mol此氯代烷可与4 mol氯气发生完全的取代反应,则该烃的结构筒式为
A.CH2==CH2 B.CH3CH==CH2
C.CH3CH3 D.CH3CH2CH==CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,根据碱金属元素性质的递变规律预测其性质,其中不正确的是 ( )
A.在碱金属元素中它具有最大的原子半径
B.钫在空气中燃烧时,只生成化学式为Fr2O的氧化物
C.它的氢氧化物的化学式为FrOH,这是一种极强的碱
D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
| a | |||||||
| b | c | d | |||||
| e | f | g |
(1)f元素在周期表中的位置是 ;g元素原子结构示意图为 ;
(2)e在空气中燃烧的产物所含化学键的类型为 、 ;
(3)化合物ca3的电子式为 ,ca3的催化氧化反应的化学方程式为 ;
(4)用电子式表示e与g元素形成化合物的过程 ;a与d组成18电子的分子化学式为 。
(5)a、c、d中的两种元素可组成具有10个电子的多种分子和离子,写出其中两种离子反应生成两种分子的离子方程式 。
(6)由a、b、c、d四种元素中的三种元素组成的某种化合物的浓溶液,可与其中的第四种元素的单质发生反应,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物M是合成药物的中间体,其结构如右图所示,下列说法不正确的是( )
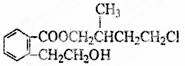 A.M属于芳香族化合物
A.M属于芳香族化合物
B.M的分子式为C14H19O3Cl
C.1 mol M最多能消耗3 mol NaOH
D.M能发生取代、加成、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)电镀时,镀件与电源的 极连接。电镀铜时,电解质溶液应选用 (填化学式)。
(1)电镀时,镀件与电源的 极连接。电镀铜时,电解质溶液应选用 (填化学式)。
(2)化学镀的原理是利用化学反应生成金属单质沉淀在镀件表面形成镀层。
①若用铜盐进行化学镀铜,应选用 (填“氧化剂”或“还原剂”)与之反应。
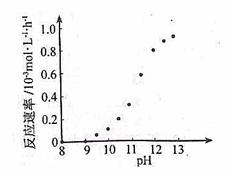
②某化学镀铜的反应速率随镀液pH变化如右图所示。该镀铜过程中,镀液pH控制在12.5左右。据图中信息,给出使反应停止的方法 。
(3)酸浸法制取硫酸铜的流程示意图如下:
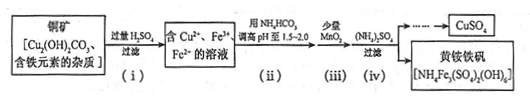
①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为 。
②步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号)。
③在步骤(iii)发生的反应中,1molMnO2转移2mol电子,该反应的离子方程式为 ______。
④步骤(iv)除去杂质的化学方程式可表示为
3 Fe3+ + NH4+ + 2SO42- + 6H2O = NH4Fe 3 (SO4)2 (O H ) 6 ↓ + 6H+
过滤后母液的pH=2.0,c(Fe3+)=a mol·L-1,c(NH4+)=b mol·L-1,c(SO42-)=d mol·L-1,该反应的平衡常数K= (用含a、b、d的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O(l)时,放出445 kJ热量,则下列热化学方程式中正确的是
A.2CH4(g)+4O2(g)===2CO2(g)+4H2O(l) ΔH=+890 kJ/mol
B.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=+890 kJ/mol
C.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ/mol
D.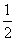 CH4(g)+O2(g)===
CH4(g)+O2(g)===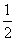 CO2(g)+H2O(l) ΔH=-890 kJ/mol
CO2(g)+H2O(l) ΔH=-890 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com