
分析 NH3溶于水后虽然大部分生成NH3•H2O,但在计算时,仍以NH3作为氨水中的溶质,设水的体积为1L,则氨气的体积为560L,根据n=$\frac{V}{{V}_{m}}$计算氨气的物质的量,根据m=nM计算氨气质量,根据m=ρV计算水的质量,溶液质量=氨气质量+水的质量,根据质量分数=$\frac{溶质质量}{溶液质量}$×100%计算该氨水的质量分数,再根据c=$\frac{1000ρω}{M}$计算氨水的物质的量浓度.
解答 解:(1)NH3溶于水后虽然大部分生成NH3•H2O,但在计算时,仍以NH3作为氨水中的溶质;
设水的体积为1L,氨气的体积为560L,
则氨气的物质的量为=$\frac{560L}{22.4L/mol}$=25mol,
氨气的质量为25mol×17g/mol=425g,
1L水的质量=1L×1000g/L=1000g,
溶液的质量为1000g+425mol=1425g,
则氨水的质量分数为w=$\frac{425g}{1425g}$×100%=29.8%,
答:该氨水的质量分数为29.8%.
(2)氨水的物质的量浓度为c=$\frac{1000×0.9×29.8%}{17}$mol/L=15.8 mol/L,
答:溶液的物质的量浓度为15.8mol/L.
点评 本题考查物质的量浓度和质量分数的计算,难度中等,注意理解掌握物质的量浓度与质量分数之间关系,可以利用定义法计算溶液物质的量浓度,计算溶液的体积是关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
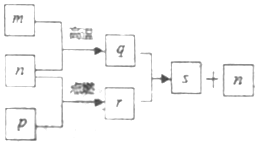 短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 化合物Z2Y2与X2Y2中化学键完全相同 | |
| B. | 最简单氢化物的沸点:Y>W | |
| C. | 36g物质q与过量的物质r反应则有2mol电子发生转移 | |
| D. | 由Y、Z、W三种元素组成的化合物的水溶液一定显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将等体积、等物质的量浓度的CH3COONH4与CH3COONa溶液混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 0.1mol•L-1pH为4的NaHA溶液中:c(HA-)>c(H2A)>c(A2-) | |
| C. | 物质的量浓度相等的①NH4Cl ②(NH4)2SO4 ③NH4Al(SO4)2三种溶液中,c(NH4+)由大到小的顺序为:③>②>① | |
| D. | 向0.10mol•L-1 Na2CO3溶液中通入少量CO2的溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常情况下,1.5molO2的体积约为33.6L | |
| B. | NaOH的摩尔质量是40g | |
| C. | 100 mL水中溶解5.85gNaCl所得NaCl溶液的物质的量浓度为1 mol•L-1 | |
| D. | 任何条件下,等物质的量的水和一氧化碳所含有的分子数必相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8:3 | B. | 2:3 | C. | 3:4 | D. | 3:8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂,在单位时间内提高合成氨产率 | |
| B. | 对于2HI(g)?H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颇色变深 | |
| C. | 对于2CaO2(s)?2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变 | |
| D. | 溴水中有下列平衡:Br(aq)+H2O(l)?HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,60g甲醛、乙酸与葡萄糖混合物充分燃烧消耗氧气分子数为3NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1 mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5 mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA | |
| D. | 142 g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com