
| Cu或Ag |
| △ |
| Cu或Ag |
| △ |
| FeBr3 |
| FeBr3 |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
| X | Y |
| W | Z |
| A、若Z的核电荷数是Y的两倍,则X为碳元素 |
| B、若W的核电荷数是Y的两倍,则X是氮元素 |
| C、原子半径:Z>Y>X |
| D、最简单氢化物的稳定性:Y>X>W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在1L0.1mol/L碳酸钠溶液中,阴离子总数大于0.1 NA |
| B、1molCaC2中含有阴离子数目为2NA |
| C、120gNaHSO4在水溶液和熔融状态下电离出来的离子总数均为3NA |
| D、2mol SO2和1 mol O2混合气体在V2O5存在的条件下于密闭容器中加热反应后容器内物质分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁粉和氯化铁溶液反应 Fe+2Fe3+→3Fe2+ |
| B、铁和稀盐酸反应 2Fe+6H+→2Fe3++H2↑ |
| C、硫化亚铁溶于稀硝酸中:FeS+2H+→Fe2++H2S↑ |
| D、铝和氢氧化钠溶液反应 2Al+2OH-→2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组合分类 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 纯碱 | 盐酸 | 烧碱 | 氧化铝 | 二氧化碳 |
| B | 烧碱 | 硫酸 | 食盐 | 氧化镁 | 一氧化碳 |
| C | 苛性钠 | 醋酸 | 碳酸铵 | 过氧化钠 | 二氧化硫 |
| D | 苛性钾 | 盐酸 | 小苏打 | 氧化钠 | 三氧化硫 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、① | B、② | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
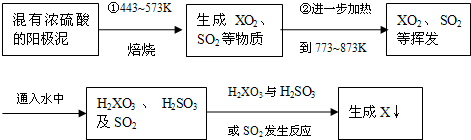
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com