
【题目】pH值相等的盐酸(甲)和醋酸(乙),盐酸与醋酸浓度的大小关系是( )
A. 甲=乙 B. 甲<乙 C. 甲>乙 D. 不确定
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是均含有氮元素的化合物,其中A是红棕色的气体,F能使红色湿润石蕊试纸变蓝色,它们之间能发生如下反应:
① A+H2O → B+C ② C+F → D ③ D+NaOH → F+E+H2O
(1)写出它们的化学式:D_______________,F_______________。
(2)写出①反应的化学方程式:_______________________________
(3)写出反应③的离子方程式:___________________________。
(4)工业生产C的过程中有如下一步反应:即F经催化氧化生成B和H2O,写出该步反应的化学方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是21世纪应用最广泛的清洁燃料之一,通过以下反应可以制备甲醇:
CO(g)+2H2(g)=CH3OH(l) △H=?
(1)已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1453.0kJ·mol-1
则制备甲醇反应的△H = kJ·mol-1
(2)若装置为容积固定的密闭容器,不同时间段各物质的浓度如下表:
c(CO) /mol·L-1 | c(H2) /mol·L-1 | c(CH3OH) /mol·L-1 | |
0min | 0.8 | 1.6 | 0 |
2min | 0.6 | y | 0.2 |
4min | 0.3 | 0.6 | 0.5 |
6min | 0.3 | 0.6 | 0.5 |
反应从2min到4min之间,H2的平均反应速率为________ mol·Lˉ1·minˉ1。
反应在第2min时改变了反应条件,改变的条件可能是 (填字母序号)。
A.使用催化剂 B.降低温度 C.增加H2的浓度 D.减小CH3OH(g)的浓度
(3)若在容积可变的密闭容器中充入1 mol CO(g)和2 molH2 (g)生成CH3OH(g),H2的平衡转化率随温度(T)、压强(P)的变化如图所示。当达到平衡状态A 时,容器的体积为2 L,此时该反应的平衡常数为 ,若达到平衡状态B 时,则容器的体积V(B)= L。
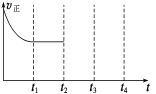
(4)一定温度下,在容积固定的密闭容器中充入一定量的H2和CO,在t1时达到平衡。t2时将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时达到新的平衡状态,之后不再改变条件。请在右图中补画出从t2到t4正反应速率随时间的变化曲线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两物质作用时,反应条件或反应物用量的改变,对生成物没有影响的是( )
A.Na2O2和CO2 B.Na和O2 C.NaOH 和CO2 D.C和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于可逆反应的是( )
A. Fe + CuCl2﹦FeCl2 + Cu B. 2 Na + 2H2O = 2NaOH + H2↑
C. 2H2 + O2![]() 2H2O D. H2+I2
2H2O D. H2+I2 ![]() 2HI
2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A.把NaHCO3和Na2CO3混和物6.85 g溶于水制成100 mL溶液,其中c(Na+)=1 mol·L-1,该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量无法计算
B.将54.4 g铁粉和氧化铁的混合物中加入4.0mol/L200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况),反应后的溶液中滴加KSCN不显红色,且无固体剩余物,反应后得到FeSO4的物质的量是0.8mol
C.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生,达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
D.某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42+ 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是H+、NH4+、Mg2+、Al3+

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯水,升温,c(H+)(),KW(),溶液呈()性
A. 变大 变小 酸性 B. 变大 变大 中性 C. 变小 变大 碱性 D. 变小 变小 中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4 molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3 molL-1s-1
②物质 B的体积分数是40%
③2 s 时物质 A 的转化率为30%
④2 s 时物质 B 的浓度为 1.0 molL-1
其中正确的是
A. ①④ B. ②③ C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2OH+NaBr+H2SO4(浓)![]() CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
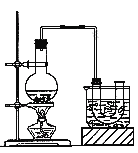
①按下图所示连接仪器,检查装置的气密性,然后向U形管和大烧杯里加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小火加热,使其充分反应。
(1)反应时若温度过高可看到有红棕色气体产生,该气体的化学式为 。
(2)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是____ ______。
(3)反应结束后,U形管中粗制的溴乙烷呈棕黄色。将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,分液,取下层液体。为了除去其中的杂质,可选择下列试剂中的 (填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
(4)要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行 (填操作名称)。
(5)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:取少量溴乙烷,然后 (填序号)。
①加入AgNO3溶液 ②加入稀HNO3酸化③冷却④加热⑤加入NaOH溶液上述实验过程中C2H5Br发生的反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com